达克替尼(Vizimpro)的说明书
达克替尼是一种口服的酪氨酸激酶抑制剂,主要用于一线治疗具有特定EGFR基因突变的转移性非小细胞肺癌(NSCLC)患者。EGFR是一种细胞表面受体,参与了细胞生长、分化和存活等过程。在一些NSCLC患者中,存在EGFR基因的特定突变(如外显子19缺失或外显子21L858R替代突变)。这些突变导致EGFR信号通路异常活跃,进而促进肿瘤细胞的生长和扩散。目前已经在国内上市,本文就达克替尼的适应症、用法用量、副作用、禁忌、临床疗效等进行了详细说明。
(一)适应症
达克替尼适用于通过FDA批准的试验检测到的具有表皮生长因子受体(EGFR)外显子19缺失或外显子21L858R替代突变的转移性非小细胞肺癌癌症(NSCLC)患者的一线治疗。

达克替尼
(二)用法用量
1.患者选择
根据肿瘤标本中EGFR外显子19缺失或外显子21L858R替代突变的存在,选择接受达克替尼一线治疗转移性NSCLC的患者。
2.推荐剂量
(1)达克替尼的推荐剂量为45mg,每天口服一次,直到出现疾病进展或不可接受的毒性。达克替尼可以与食物一起服用,也可以不一起服用。
(2)每天同一时间服用达克替尼。如果患者出现呕吐或错过了一剂,不需要再服用一剂或补上错过的剂量,而是继续服用下一剂计划剂量。
3.不良反应的剂量调整
如表1所述,减少达克替尼的不良反应剂量。表2中提供了特定不良反应的剂量调整。
表1.达克替尼出现不良反应时建议减少的剂量

表2.针对不良反应的达克替尼剂量调整
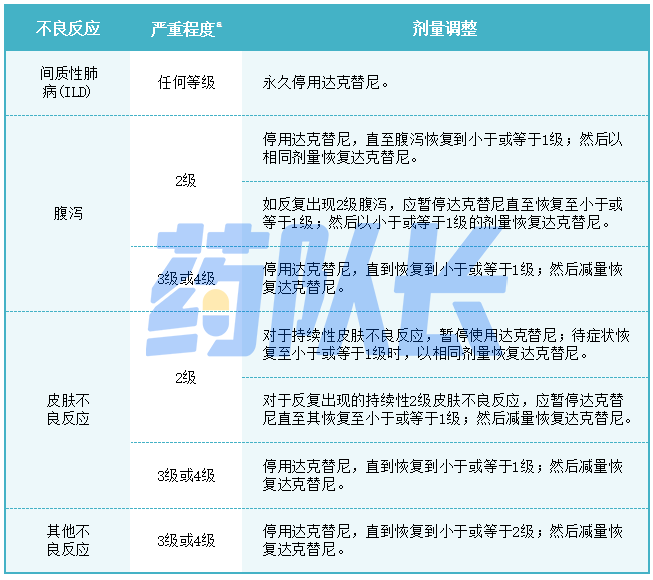
a国家癌症研究所不良事件通用术语标准4.03版。
4.减酸剂的剂量调整
在服用达克替尼时避免同时使用质子泵抑制剂(PPI)。作为PPIs的替代品,使用局部作用抗酸剂,或者如果使用组胺2(H2)受体拮抗剂,则在服用H2受体拮抗剂之前至少6小时或之后至少10小时给予达克替尼。
5.肾损害患者的剂量调整
不建议对轻度或中度肾功能损害(依据Cockcroft-Gault公式预计肌酐清除率[CLcr]在30~89mL/min)的患者调整剂量。尚未确定重度肾功能损害(CLcr<30mL/min)患者的达克替尼推荐剂量。
6.肝损害患者的剂量调整
不建议对轻度(总胆红素≤正常上限[ULN]且AST>ULN,或总胆红素>1至1.5×ULN伴任何AST)或中度(总胆红素>1.5至3×ULN伴任何AST)肝损害的患者调整剂量。尚未确定重度肝损害(总胆红素>3至10×ULN伴任何AST)患者的推荐剂量。
(三)适用人群
成人。儿童、哺乳期妇女及年老体弱者应在医生指导下使用。
(四)禁忌
尚未明确。
(五)副作用
最常见的不良反应(发生率>20%)是腹泻、皮疹、甲沟炎、口腔炎、食欲下降、皮肤干燥、体重下降、脱发、咳嗽和瘙痒。
(六)注意事项
1.间质性肺病(ILD)
(1)使用达克替尼治疗的患者曾发生过严重和致命的ILD/肺炎,其在394名接受达克替尼治疗的患者中发生率为0.5%;其中,0.3%的病例致死。
(2)监测患者预示ILD/肺炎的肺部症状。在呼吸系统症状恶化且可能预示ILD(例如呼吸困难、咳嗽和发热)的患者中暂时停用达克替尼并立即进行ILD的诊断。如果确诊为任何级别的ILD,则永久停用达克替尼。
2.腹泻
(1)使用达克替尼治疗的患者曾发生过严重和致命的腹泻。在394名接受达克替尼治疗的患者中,腹泻的发生率为86%;其中,11%的患者报告了3或4级腹泻,0.3%的病例致死。
(2)对于≥2级腹泻,请暂时停用达克替尼,直到恢复至≤1级,然后根据腹泻严重程度,按相同剂量水平或降低一个剂量水平继续服用达克替尼。对于腹泻患者,立即开始止泻治疗(洛哌丁胺或盐酸地芬诺酯与硫酸阿托品)。
3.皮肤不良反应
(1)使用达克替尼治疗的患者曾发生过皮疹和剥脱性皮肤反应。在394名接受达克替尼治疗的患者中,皮疹的发生率为78%;21%的患者报告了3或4级皮疹。7%的患者报告了不同严重程度的剥脱性皮肤反应。1.8%的患者报告了3或4级剥脱性皮肤反应。
(2)对于持续性2级或任何3或4级皮肤不良反应,请暂时停用达克替尼,直到恢复至≤1级,然后根据皮肤不良反应的严重程度,按相同剂量水平或降低一个剂量水平继续服用达克替尼。皮疹和剥脱性皮肤反应的发生率和严重程度可能会随着阳光照射而增加。开始使用达克替尼时,请同时使用保湿霜并采取适当的措施防晒。一旦发生1级皮疹后,开始使用局部抗生素和局部类固醇治疗。出现≥2级皮肤不良反应后,开始口服抗生素治疗。
4.胚胎-胎儿毒性
根据动物研究的结果及其作用机制,妊娠女性服用达克替尼可对胎儿造成伤害。在动物生殖研究中,妊娠大鼠在器官形成期间口服一定剂量(暴露量接近45mg人类用药剂量的暴露量)达克替尼后,导致着床后流产和胎儿体重下降的发生率增加。EGFR信号传导的缺失导致动物的胚胎死亡以及出生后死亡。应告知妊娠女性达克替尼对胎儿有潜在风险。建议具有生育能力的女性接受达克替尼治疗期间采取有效的避孕措施,并持续至服用最后一剂达克替尼后至少17天。
(七)治疗效果
一线达克替尼治疗EGFR突变阳性非小细胞肺癌亚洲患者的安全性和有效性
试验设计:
在这项正在进行的随机、开放标签3期试验中,符合条件的新诊断晚期EGFR突变阳性NSCLC患者被随机(1:1)接受口服达克替尼45mg/天或口服吉非替尼250毫克/天。通过中央计算机系统进行随机化,按种族和EGFR突变类型进行分层。主要终点是通过盲法独立审查得出的PFS。
试验结果:
在346名亚洲患者中,170名被随机分配至达克替尼,176名被随机分配至吉非替尼。达克替尼与吉非替尼的PFS风险比(HR)为0.509。达克替尼与吉非替尼的OSHR为0.759。逐步减少达克替尼剂量(至30和15毫克/天)的患者仍保持OS获益。达克替尼最常见的不良事件(AE)为腹泻(154例[90.6%]患者)、甲沟炎(110例[64.7%])、痤疮样皮炎(96例[56.5%])和口腔炎(87例[51.2%])。吉非替尼治疗后出现腹泻(100[56.8%])、丙氨酸转氨酶升高(81[46.0%])和天冬氨酸转氨酶升高(75[42.6%])。
试验结论:
在EGFR突变阳性晚期NSCLC亚洲患者中,与吉非替尼相比,一线达克替尼与PFS显着延长和OS改善相关。亚洲患者中达克替尼和吉非替尼的AE特征与ARCHER1050总体人群一致。
(八)药物相互作用
1.其他药物对达克替尼的影响
与PPI同时使用会降低达克替尼的浓度,从而可能降低达克替尼的疗效。避免达克替尼与PPI同时使用。可使用局部作用的抗酸剂或H2受体拮抗剂,作为PPI的替代品。在服用H2受体拮抗剂至少6小时前或至少10小时后给予达克替尼。
2.达克替尼对CYP2D6底物的影响
同时使用达克替尼会增加CYP2D6底物药物的浓度,从而可能增加这些药物的毒性风险。避免同时使用达克替尼与CYP2D6底物,因为CYP2D6底物浓度略微增加可能产生严重的或危及生命的毒性。
(九)储存条件
达克替尼为蓝色薄膜衣片,除去包衣后显白色或类白色。
30℃以下保存。
【温馨提示】:部分商品说明书更换频繁,请以商品实物为准。

- 【非小细胞肺癌】SH-1028片[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- 【食管鳞癌】LY01015注射液联合氟尿嘧啶和顺铂[适 应 症]晚期或转移性食管鳞癌[试验分期]Ⅲ期
- 【黑色素瘤】GT101注射液[适 应 症]一线治疗失败的宫颈鳞癌或恶性黑色素瘤患者[试验分期]Ⅰ期
- 【实体瘤】注射用TFX05-01[适 应 症]本品拟用于经病理组织/细胞学或临床诊断确诊,不适合手术或局部治疗, 或经过手术和/或经末线标准治疗后疾病进展和/或无法耐受标准治疗的晚期恶性实体瘤患者。[试验分期]Ⅰ期
- 【实体瘤】BC007抗体注射液[适 应 症]CLDN18.2表达的晚期实体瘤[试验分期]Ⅰ期
- 【淋巴瘤】MIL62注射液联合来那度胺胶囊[适 应 症]难治的滤泡性淋巴瘤[试验分期]Ⅲ期