培米替尼(pemazyre)的说明书
培米替尼是一种靶向性药物,用于治疗胆管癌和伴有FGFR1基因重排的髓细胞/淋巴细胞肿瘤。它通过抑制FGFR1受体的活化,干预肿瘤细胞的异常信号通路,从而达到抑制肿瘤生长和转移的目的。然而,使用前仍需遵循医生的建议,并了解可能的副作用和风险。本文就培米替尼的适应症、用法用量、副作用、禁忌、临床疗效等进行了详细说明。
(一)适应症
1.胆管癌
培米替尼适用于治疗经FDA批准的试验检测出成纤维细胞生长因子受体2(FGFR2)融合或其他重排的、既往接受过治疗但无法切除的局部晚期或转移性胆管癌成人患者。
2.伴有FGFR1基因重排的髓细胞/淋巴细胞肿瘤
培米替尼适用于治疗伴有成纤维细胞生长因子受体1(FGFR1)重排的复发性或难治性髓/淋巴肿瘤(MLN)成人患者。
培米替尼的图片
(二)用法用量
1.患者的选择
(1)根据FDA批准的检测方法检测出的FGFR2融合或重排情况,选择使用培米替尼治疗局部晚期或转移性胆管癌的患者。
(2)根据FGFR1基因重排的存在,选择患者使用培米替尼治疗复发或难治性骨髓/淋巴肿瘤。目前尚无美国FDA批准的用于检测复发或难治性髓/淋巴肿瘤患者FGFR1基因重排的检测方法,以选择接受培米替尼治疗的患者。
2.推荐剂量
培米替尼的用法用量
(1)每天大约在同一时间与食物一起或不与食物一起服用培米替尼。
(2)整片吞服。请勿压碎、咀嚼、分割或溶解药片。
(3)如果患者错过服用培米替尼4小时或4小时以上或发生呕吐,则应在下一次预定剂量时继续服用。
胆管癌
培米替尼的推荐剂量为13.5mg,口服,每天一次,连续14天,然后停药7天,21天为一个周期。继续治疗直至疾病进展或出现不可接受的毒性反应。
伴有FGFR1基因重排的骨髓性/淋巴性肿瘤
培米替尼的推荐剂量为13.5mg,每日口服一次,连续服用。继续治疗直至疾病进展或出现不可接受的毒性。
3.不良反应的剂量调整
表一 不良反应的剂量调整

*如果不能耐受4.5mg,每天一次,每21天周期的前14天,则永久停用培米替尼
表二 不良反应的剂量调整

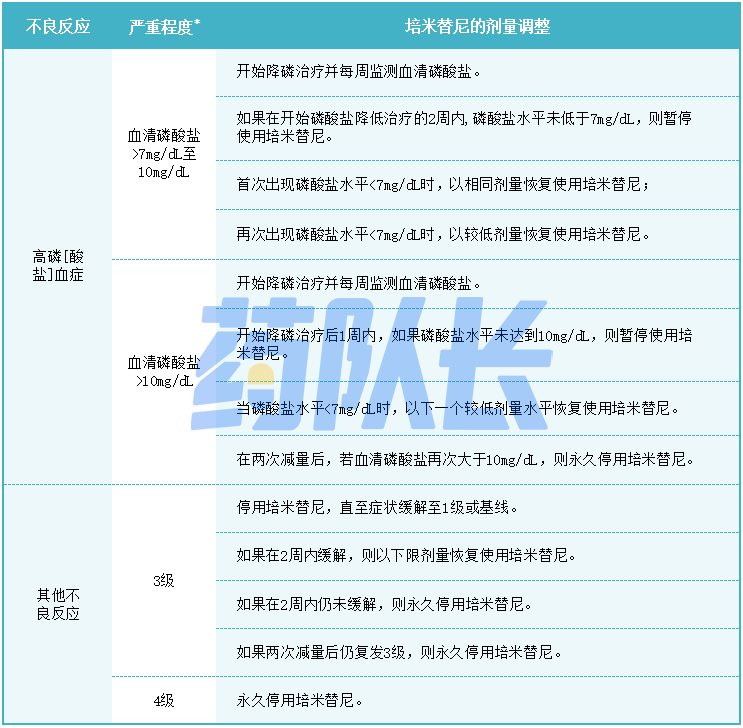
*严重程度由美国国家癌症研究所不良事件通用术语标准(NCICTCAE)4.03版定义
4.与强或中度CYP3A抑制剂同时使用的剂量调整
(1)培米替尼应避免同时使用强效和中效CYP3A抑制剂。如果无法避免与强效或中效CYP3A抑制剂同时使用:
①将培米替尼的用量从13.5mg减至9mg。
②将培米替尼的用量从9mg减至4.5mg。
(2)如果停止同时使用强效或中效CYP3A抑制剂,则将培米替尼的用量(在CYP3A抑制剂的3个血浆半衰期之后)增加到开始使用强效或中效抑制剂之前的用量。
5.严重肾功能损害的推荐剂量
严重肾功能损害患者(根据肾病饮食改良法[MDRD]估计的eGFR为15mL/min/1.73m2至29mL/min/1.73m2)的培米替尼推荐剂量为9mg,并根据适应症指定用药计划(间歇或持续用药)。
6.重度肝功能损害的推荐剂量
严重肝功能损害患者(总胆红素>3倍正常值上限(3×ULN)且伴有任何谷草转氨酶升高)的培米替尼推荐剂量为9mg,并按照适应症指定的时间表(间歇或持续)服用。
(三)适用人群
成人。妊娠期、哺乳期女性,以及老人和儿童患者在医生指导下用药。
(四)禁忌
尚未明确
(五)副作用
1.胆管癌最常见的不良反应(≥20%)
高磷血症、脱发、腹泻、指甲毒性、疲劳、吞咽困难、恶心、便秘、口炎、干眼、口干、食欲下降、呕吐、关节痛、腹痛、低磷血症、背痛和皮肤干燥。
2.髓系/淋巴系肿瘤伴FGFR1重排最常见的不良反应(≥20%)
高磷血症、指甲毒性、脱发、口炎、腹泻、干眼、疲劳、皮疹、腹痛、贫血、便秘、口干、鼻出血、浆液性视网膜脱离、四肢疼痛、食欲减退、皮肤干燥、消化不良、背痛、恶心、视力模糊、周围水肿和头晕。
(六)注意事项
1.眼毒性
(1)视网膜色素上皮脱离(RPED)
①培米替尼可引起视网膜色素上皮脱离(RPED),可能会导致视力模糊、视觉漂浮物或视光症等症状。
②在开始使用培米替尼之前,进行一次全面的眼科检查,包括OCT,在治疗期间,头6个月每2个月检查一次,此后每3个月检查一次。出现视觉症状时,应立即转诊进行眼科评估,每3周进行一次随访,直至症状缓解或停用培米替尼。
(2)干眼
培米替尼可引起干眼症,根据需要给患者使用眼部镇痛药。
2.高磷酸盐血症与软组织矿化
(1)培米替尼可引起高磷血症,导致软组织矿化、皮肤钙化、钙化和非尿毒症性钙化。
(2)当血清磷酸盐水平>5.5mg/dL时,监测高磷血症并开始低磷饮食。如果血清磷酸盐水平>7mg/dL,则启动降磷治疗,并根据高磷血症的持续时间和严重程度暂停、减少剂量或永久停用培米替尼。
3.胚胎-胎儿毒性
(1)孕妇服用培米替尼可能会对胎儿造成伤害。
(2)告知孕妇胎儿可能面临的风险。建议具有生育能力的女性患者在使用培米替尼治疗期间及最后一次用药后1周内采取有效的避孕措施。告知有女性生育伴侣的男性患者在使用培米替尼治疗期间及最后一次用药后1周内采取有效的避孕措施。
(七)治疗效果
培米替尼治疗骨髓/淋巴肿瘤伴FGFR1重排的试验
1.试验设计
FIGHT-203(NCT03011372)是一项多中心、开放标签、单臂试验,评估了培米替尼在28例伴有FGFR1重排的mln患者中的疗效。
2.试验结果及试验结果的设定
(1)在伴有或不伴有髓外疾病(EMD)的骨髓慢性期患者中,根据完全缓解(CR)确定疗效。CR是根据MDS/MPN工作组对MDS/MPN肿瘤的反应标准(2015年)定义的,附加要求外周嗜酸性粒细胞<0.5×109/L,如果相关,则使用Lugano标准定义EMD中的CR(Cheson2014)。CR率为78%。CR缓解的中位时间为104天。CR的中位持续时间未达到。
(2)在有或没有EMD的骨髓母细胞期患者中,根据CR来确定疗效,CR定义为骨髓母细胞<5%,无疾病证据,外周血计数完全恢复(血小板>10万/微升,绝对中性粒细胞>1000/微升)。在4例blast期患者中,2例患者达到CR。
(3)仅在EMD患者中,根据Lugano标准(Cheson2014)的CR确定疗效。1例患者达到CR(持续时间:64天以上)。
(4)所有患者(包括3例无形态学疾病证据的患者),完全细胞遗传学缓解率为79%。
(八)药物相互作用
1.强效和中效CYP3A诱导剂
(1)培米替尼与强效或中效CYP3A诱导剂同时使用会降低pemigatinib的血浆浓度,从而可能降低培米替尼的疗效。避免同时使用强效和中效CYP3A诱导剂与培米替尼。
(2)CYP3A强诱导剂:利福平(抗结核)、利福喷丁:(结核麻风{抗金黄葡萄球菌})、苯妥英(抗癫痫、抗心律失常、三叉神经痛{精神类})、卡马西平(癫痫三叉神经痛{镇痛药})、巴比妥(抑制中枢神经系统、抗惊厥、抗癫痫)、圣约翰草(治疗抑郁症焦虑烦躁、失眠)
2.强效和中效CYP3A抑制剂
(1)与培米替尼同时使用强效或中效CYP3A抑制剂会增加pemigatinib的血浆浓度,这可能会增加不良反应的发生率和严重程度。避免同时使用强效和中效CYP3A抑制剂与培米替尼。如果无法避免同时使用强效和中效CYP3A抑制剂,请减少培米替尼的用量。
(2)CYP3A强抑制剂:伊曲康唑(广谱抗真菌药)、酮康唑(广谱抗真菌药)、伏立康唑(广谱抗真菌药)、阿扎那韦(艾滋)、利托那韦(抗病毒)、克拉霉素(抗生素)
(九)储存条件
片剂储存在20℃到25℃的室温下,允许在15℃到30℃的温度下运输。
【温馨提示】:部分商品说明书更换频繁,请以商品实物为准。

- 【非小细胞肺癌】SH-1028片[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- 【食管鳞癌】LY01015注射液联合氟尿嘧啶和顺铂[适 应 症]晚期或转移性食管鳞癌[试验分期]Ⅲ期
- 【黑色素瘤】GT101注射液[适 应 症]一线治疗失败的宫颈鳞癌或恶性黑色素瘤患者[试验分期]Ⅰ期
- 【实体瘤】注射用TFX05-01[适 应 症]本品拟用于经病理组织/细胞学或临床诊断确诊,不适合手术或局部治疗, 或经过手术和/或经末线标准治疗后疾病进展和/或无法耐受标准治疗的晚期恶性实体瘤患者。[试验分期]Ⅰ期
- 【实体瘤】BC007抗体注射液[适 应 症]CLDN18.2表达的晚期实体瘤[试验分期]Ⅰ期
- 【淋巴瘤】MIL62注射液联合来那度胺胶囊[适 应 症]难治的滤泡性淋巴瘤[试验分期]Ⅲ期