瑞博西尼的用法用量是什么?
瑞博西尼是一种治疗乳腺癌的药物,在使用时需要遵循医生的指导和推荐剂量。准确的剂量选择对于确保疗效和最小化不良反应非常重要。实际的剂量可能因患者的具体情况而有所不同,如年龄、体重、肝功能和肾功能等影响因素。因此,在开始使用瑞博西尼之前,患者应该与医生进行详细的讨论和评估,以确定最合适的剂量。
瑞博西尼的用法用量
1.推荐剂量
(1)瑞博西尼的推荐剂量为600mg(3片200mg薄膜包衣片)口服,每天一次,连续21天,然后停止治疗7天,形成28天的完整周期。瑞博西尼可伴餐或不伴餐服用。
(2)当使用瑞博西尼时,请参阅完整处方信息,了解所使用的芳香酶抑制剂的推荐剂量。
(3)当与瑞博西尼联合给药时,氟维司群的推荐剂量为500mg,分别在第1、15、29天给药,此后每月给药一次。请参阅氟维司群的完整处方信息。
(4)根据目前的临床实践标准,使用瑞博西尼加芳香化酶抑制剂联合治疗的绝经前/围绝经期女性或男性应使用促黄体生成素释放激素(LHRH)激动剂。
(5)根据目前的临床实践标准,使用瑞博西尼加氟维司群联合治疗的男性应使用促黄体生成素-释放激素(LHRH)激动剂。
(6)患者应在每天大约相同的时间服用瑞博西尼,最好是在早晨。
(7)如果患者在服药后呕吐,或漏服一剂,当天不应再服用额外剂量。下一个处方剂量应在正常时间服用。
(8)瑞博西尼片剂应整片吞下(吞咽前不应咀嚼、压碎或分裂)。如果药片破碎、破裂或不完整,则不应服用。
2.剂量调整
(1)不良反应的剂量调整
表1列出了针对不良反应的剂量调整。
表1:针对不良反应的推荐剂量修改
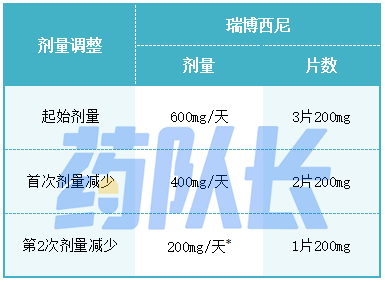
*:如果需要进一步将剂量减少至200mg/天以下,请停止用药。
表2、3、4、5、6和7总结了在处理特定不良反应时中断、减少或停用瑞博西尼的建议。建议根据个体安全性和耐受性调整瑞博西尼的剂量。
表2:间质性肺疾病/肺炎的剂量调整和管理
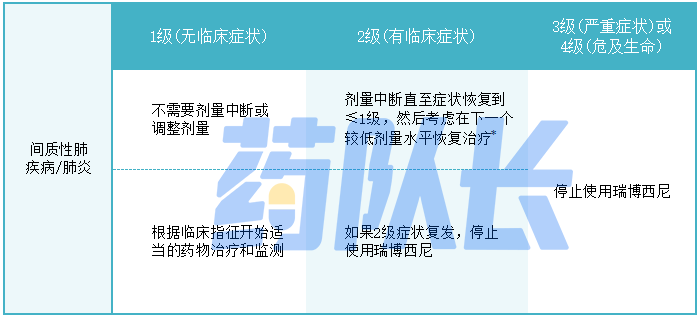
根据不良事件通用术语标准(CTCAE)4.03版进行分级。
*:在考虑恢复瑞博西尼时,应进行个体化的获益-风险评估。
表3:皮肤不良反应(包括疤痕)的剂量调整和管理

缩写:BSA,体表面积;疤痕、严重皮肤不良反应;SJS:史蒂文斯-约翰逊综合征;TEN:中毒性表皮坏死松解症
*:SJS(3级和4级)定义为皮肤脱落覆盖<10%BSA和10%-30%BSA,并伴有相关体征(例如红斑、紫癜、表皮脱离和粘膜脱离)。
**:TEN(4级)定义为皮肤脱落覆盖≥30%BSA并伴有相关症状(例如红斑、紫癜、表皮脱离和粘膜脱离)。
根据不良事件通用术语标准(CTCAE)4.03版进行分级。
表4:QT间期延长的剂量调整和管理

开始治疗前应评估心电图(ECG)。
根据临床指示,在第一个周期的第14天左右和第二个周期开始时重复心电图检查。
如果治疗期间任何给定时间出现(QTcF)延长,建议更频繁地进行心电图监测。
*:QTcF=通过Fridericia公式校正的QT间期。
表5:肝胆毒性的剂量调整和管理

在开始使用瑞博西尼治疗之前进行肝功能测试(LFT)。
对于前2个周期,每2周监测一次肝功能测试,在随后的每4个周期开始时以及根据临床指示进行监测。
如果发现≥2级异常,建议进行更频繁的监测。
缩写:AST:天冬氨酸转氨酶;ALT:丙氨酸转氨酶;ULN:正常值上限。
*:基线=治疗开始前。
根据不良事件通用术语标准(CTCAE)4.03版进行分级。
表6:中性粒细胞减少症的剂量调整和管理

在开始使用瑞博西尼治疗之前进行全血细胞计数(CBC)。
在前2个周期中每2周监测一次全血细胞计数,在随后的每4个周期开始时以及根据临床指示进行监测。
缩写:ANC:绝对中性粒细胞计数;LLN:正常值下限。
*:3级中性粒细胞减少症:单次发烧>38.3°C(或)并持续1小时以上,和/或并发感染。根据不良事件通用术语标准(CTCAE)4.03版进行分级。
表7:其他毒性的剂量修改和管理*

*:不包括间质性肺病(ILD)/肺炎、皮肤不良反应,包括严重皮肤不良反应(SCAR)、QT间期延长、肝胆毒性和中性粒细胞减少。
根据不良事件通用术语标准(CTCAE)4.03版进行分级。
请参考芳香酶抑制剂或氟维司群的完整处方信息,了解出现毒性时的剂量调整指南和其他相关安全信息。
(2)使用强CYP3A抑制剂的剂量调整
避免瑞博西尼与强CYP3A抑制剂同时使用,并考虑使用CYP3A抑制潜力较小的替代合并用药。如果必须同时使用强CYP3A抑制剂,则将瑞博西尼剂量减少至400mg,每日一次。如果强抑制剂停用,将瑞博西尼剂量(强CYP3A抑制剂至少5个半衰期后)更改为强CYP3A抑制剂开始使用前的剂量。
(3)肝损伤的剂量调整
轻度肝功能损害(Child-Pugh A级)患者无需调整剂量。中度(Child-Pugh B级)和重度肝受损(ChildPugh C级)患者瑞博西尼的推荐起始剂量是400mg,每天一次。查看芳香酶抑制剂或氟维司群的完整处方信息,了解与肝功能损害相关的剂量调整。
(4)肾损伤的剂量调整
轻度或中度肾功能不全患者无需调整剂量。严重肾功能受损患者推荐起始剂量是200mg,每天一次。

- 【非小细胞肺癌】SH-1028片[适 应 症]非小细胞肺癌[试验分期]Ⅲ期
- 【食管鳞癌】LY01015注射液联合氟尿嘧啶和顺铂[适 应 症]晚期或转移性食管鳞癌[试验分期]Ⅲ期
- 【黑色素瘤】GT101注射液[适 应 症]一线治疗失败的宫颈鳞癌或恶性黑色素瘤患者[试验分期]Ⅰ期
- 【实体瘤】注射用TFX05-01[适 应 症]本品拟用于经病理组织/细胞学或临床诊断确诊,不适合手术或局部治疗, 或经过手术和/或经末线标准治疗后疾病进展和/或无法耐受标准治疗的晚期恶性实体瘤患者。[试验分期]Ⅰ期
- 【实体瘤】BC007抗体注射液[适 应 症]CLDN18.2表达的晚期实体瘤[试验分期]Ⅰ期
- 【淋巴瘤】MIL62注射液联合来那度胺胶囊[适 应 症]难治的滤泡性淋巴瘤[试验分期]Ⅲ期