




首个用于复发型多发性硬化症的CD20单抗
 美国TG治疗公司
美国TG治疗公司
适用于治疗复发型多发性硬化症(MS),包括临床孤立综合征、复发缓解型疾病和活动性继发进行性疾病
(1)乙型肝炎病毒筛查
在使用BRIUMVI之前,进行乙型肝炎病毒(HBV)筛查
①经乙型肝炎表面抗原(HBsAg)和抗HBV检测阳性证实的HBV活动性患者禁用BRIUMVI
②对于HBsAg阴性、乙型肝炎核心抗体[HBcAb+]阳性或HBV携带者[HBsAg+]的患者,在开始使用BRIUMVI治疗前和治疗期间,应咨询肝病专家
(2)血清免疫球蛋白
在使用BRIUMVI之前,进行定量血清免疫球蛋白检测,对于低血清免疫球蛋白的患者,在开始使用BRIUMVI治疗前,请咨询免疫学专家
(3)疫苗接种
不建议在治疗期间和停药后直至 B 细胞恢复之前接种减毒活疫苗或活疫苗,因此根据免疫指南,至少在 BRIUMVI 开始使用前 4 周接种活疫苗或减毒活疫苗,并尽可能至少在开始使用 BRIUMVI 前 2 周接种非活疫苗
(1)感染的评估
每次注射BRIUMVI前,确定是否存在活动性感染,如果是活动性感染,延迟BRIUMVI的输注,直到感染消退
(2)推荐使用本品前用药
①每次BRIUMVI输注前约30分钟静脉给予100mg甲基强的松龙(或等效口服剂量或等效皮质类固醇),以减少输注反应的频率和严重程度
②在每次BRIUMVI输注前约30-60分钟口服或静脉给予抗组胺药(如苯海拉明),以进一步减少输注反应的频率和严重程度
③还可以考虑添加退烧药(例如,对乙酰氨基酚)
(3)怀孕测试
建议在每次输注BRIUMVI之前对具有生殖潜力的女性进行妊娠试验
在经验丰富的医疗保健专业人员的密切监督下使用BRIUMVI,并获得适当的医疗支持,以管理严重反应,例如严重的输液反应
(1)首次输注:静脉输注150mg
(2)第二次输注:第一次输注后两周静脉输注450mg
(3)后续输注:第一次输注后24周静脉输注450mg,此后每24周静脉输注一次
(4)前两次输液结束后,观察患者至少一小时,除非在当前或之前的输液中观察到输液反应和/或过敏反应,否则可由医生决定对后续输液进行输液后监测
表一:推荐剂量、输注速率和输注时间
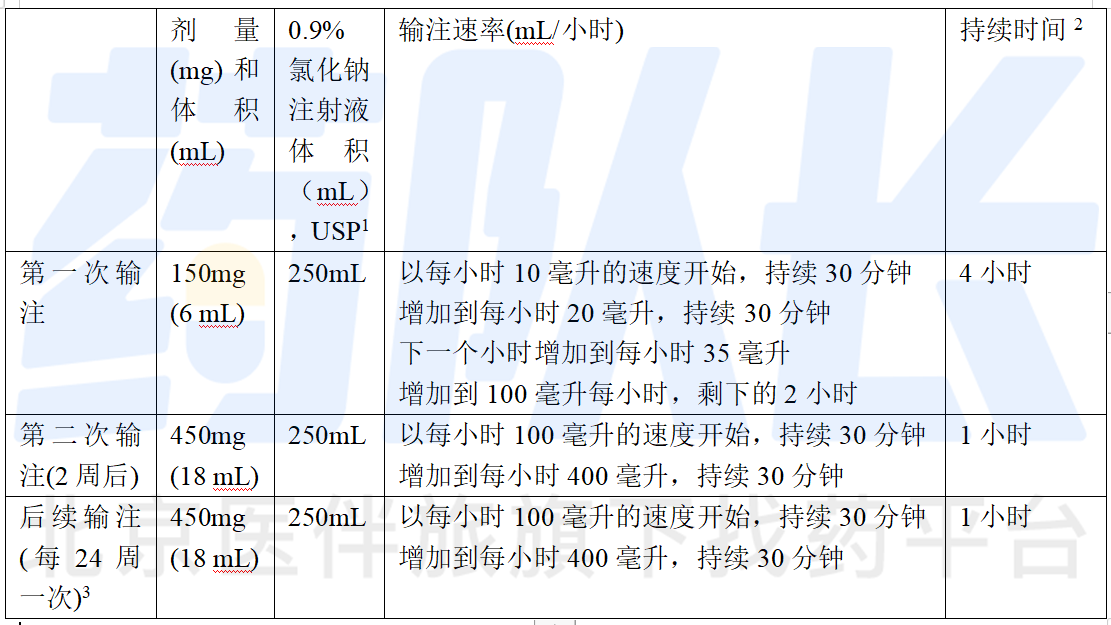
1按照制备和给药中的制备说明,从输液袋中取出并丢弃所需体积的0.9%氯化钠注射液(USP)
2如果输注中断或减慢,输注时间可能会延长
3第一次输注后24周进行第一次后续输注
如果错过了计划输注BRIUMVI,应尽快给予BRIUMVI,不要等到下一次预定的输注,重置输注计划,在错过输注24周后进行下一次连续输注,注射BRIUMVI必须至少间隔5个月
对输液反应的剂量调整取决于严重程度
(1)危及生命的输液反应
如果出现危及生命或致残的输液反应迹象,立即停止输液并永久停用BRIUMVI,提供适当的支持性治疗
(2)严重输液反应
①如有必要,立即中断输液并给予适当的支持治疗,只有在所有症状都消失后才能重新开始输液
②重新开始时,以输液反应开始时输液速率的一半开始,如果这个速率患者可以耐受,那么增加速率,如表1所示,这种速率的变化会增加输注的总持续时间,但不会增加总剂量
(3)轻度至中度输液反应
将输液速率降低到输液反应开始时速率的一半,并保持降低速率至少30分钟,如果降低的速率患者可以耐受,那么增加速率,如表1所示,这种速率的变化会增加输注的总持续时间,但不会增加总剂量
(1)制备
①仅用0.9%氯化钠注射液(USP)稀释BRIUMVI
②BRIUMVI必须由卫生保健专业人员使用无菌技术制备,按如下方法配制输注溶液:
1)BRIUMVI 应为无色至微黄色的透明至乳白色溶液,在溶液和容器允许的情况下,给药前应目测本品是否有颗粒物和变色,如果溶液变色或含有离散的外来颗粒物质,请勿使用
③第一次注射溶液的配制:
1)用一瓶BRIUMVI (150mg / 6ml)制备首次输注(150mg)输注袋
2)从 250 ml输液袋中抽出 6 ml 0.9% 氯化钠注射液,USP 并丢弃
3)从瓶中取出6ml BRIUMVI溶液
4)将6 mL (150 mg) BRIUMVI加入0.9%氯化钠注射液(USP)输液袋中
④第二次输液及后续输液溶液的配制:
1)用三瓶(150 mg/ 6ml) BRIUMVI配制输液袋,用于第二次输注(450 mg)和后续输注(450 mg)
2)从250 mL输液袋中取出18 mL 0.9%氯化钠注射液(USP)并丢弃
3)从小瓶中取出18ml BRIUMVI溶液(6ml /瓶)
4)向含有0.9%氯化钠注射液(USP)的输液袋中加入18 mL (450 mg) BRIUMVI
将稀释后的溶液温和倒置混合,不要摇晃
(2)输液给药
①开始静脉输注前,输注袋内的内容物应置于室温
②将稀释后的输液溶液通过专用管道输送
③未观察到BRIUMVI与聚氯乙烯(PVC)或聚烯烃(PO)袋和静脉(IV)给药装置之间的不兼容性
①立即使用配制好的输液液
②如果不立即使用稀释后的溶液,请在2°C至8°C(36°F至46°F)下冷藏保存24小时,不要冷冻
③如果稀释后的溶液冷藏保存,在给药前(大约2小时)使其平衡至室温
④稀释后的溶液可在室温25°C(77°F)下额外保存8小时,其中包括平衡时间和输注时间
最常见的不良反应(≥10%)是输液反应和上呼吸道感染
禁用于以下患者:
1、活动性HBV感染
2、曾因使用 BRIUMVI 而出现危及生命的输液反应
原包装储存在2°C至8°C,避光保存,不要冷冻,不要摇晃
成人。儿童、哺乳期妇女及年老体弱者应在医生指导下使用
1、BRIUMVI与其他免疫调节或免疫抑制药物(包括免疫抑制剂量的皮质类固醇)同时使用可能会增加感染的风险
2、当与BRIUMVI共同使用免疫抑制疗法时,考虑到附加免疫系统效应的风险
3、当从具有免疫效应的疗法转换时,应考虑这些疗法的持续时间和作用机制,因为在启动BRIUMVI时可能存在附加性免疫抑制效应
24个月
注射剂
美国TG治疗公司
Ublituximab-xiiy
透明至乳白色,无色至微黄色溶液,单剂量瓶装
(1)BRIUMVI可引起输液反应,包括发热、寒战、头痛、流感类疾病、心动过速、恶心、喉咙刺激、红斑和过敏反应
(2)观察BRIUMVI治疗患者在输注过程中以及前两次输注完成后至少1小时内的输注反应,后续输液的输液后监测由医生自行决定,除非观察到与当前或任何先前输液相关的输液反应和/或过敏反应,告知患者输注反应可能在输注后24小时内发生
(3)降低输液反应的风险和管理输液反应
①给药前(如甲基强的松龙或等效皮质类固醇和抗组胺药),以减少输液反应的频率和严重程度,也可以考虑添加退烧药(如对乙酰氨基酚)
②输液的管理建议取决于反应的类型和严重程度,对于危及生命的输液反应,应立即停止输液,永久停用BRIUMVI,并给予适当的支持治疗
③对于不太严重的输液反应,管理可能包括暂时停止输液,降低输液速度
在接受BRIUMVI治疗的患者中有严重的,包括危及生命或致命的细菌和病毒感染的报告,对于活动性感染患者,延迟BRIUMVI给药,直至感染消除
(1)其他免疫抑制剂可能增加免疫抑制剂作用的风险
在免疫抑制治疗后启动BRIUMVI或在BRIUMVI后启动免疫抑制治疗时,应考虑免疫抑制效应增加的可能性,BRIUMVI尚未与其他多发性硬化症疗法联合研究
(2)乙型肝炎病毒(HBV)再激活
在开始用BRIUMVI治疗前对所有患者进行HBV筛查,对于经HBsAg和抗hb试验阳性证实的HBV活动性患者,不要开始使用BRIUMVI治疗,对于表面抗原[HBsAg]阴性、HB核心抗体[HBcAb+]阳性或HBV携带者[HBsAg+]的患者,在开始治疗前和治疗期间应咨询肝病专家
(3)进行性多灶性脑白质病(PML)
与进行性多灶性脑白质病(PML)相关的典型症状多种多样,病程持续数天至数周,包括身体一侧进行性无力或四肢笨拙,视力障碍,思维、记忆和方向改变,导致混乱和人格改变,磁共振成像(MRI)的发现可能在临床症状或体征之前就很明显,因此,磁共振成像监测可能与进行性多灶性脑白质病一致的体征可能是有用的,任何可疑的发现都应进一步调查,以便早期诊断进行性多灶性脑白质病
(4)疫苗接种
根据免疫指南,在接种BRIUMVI活疫苗或减毒活疫苗至少4周前进行所有免疫接种,如有可能,在接种BRIUMVI非活疫苗至少2周前进行免疫接种,BRIUMVI可能会干扰非活疫苗的效力
①在怀孕期间接受BRIUMVI治疗的母亲所生婴儿的疫苗接种
1)在怀孕期间暴露于BRIUMVI的母亲的婴儿,在确认通过CD19+ b细胞测量的b细胞计数恢复之前,不要接种活疫苗或减毒活疫苗,这些婴儿b细胞的消耗可能会增加活疫苗或减毒活疫苗的风险
2)在b细胞耗竭恢复之前,可按指示接种灭活疫苗或非活疫苗,但应考虑评估疫苗免疫反应,包括咨询合格的专家,以确定是否产生了保护性免疫反应
建议在每次输注BRIUMVI前对具有生殖潜力的女性进行妊娠试验,建议有生殖潜力的女性在BRIUMVI治疗期间和最后一次服药后6个月内使用有效避孕措施
在治疗期间,尤其是在机会性感染或复发性感染患者中,以及在停药后直至 B 细胞补充前,监测血清免疫球蛋白的定量水平,如果免疫球蛋白过低的患者出现严重的机会性感染或复发性感染,或如果长期低丙种球蛋白血症需要使用静脉免疫球蛋白治疗,则应考虑停止 BRIUMVI 治疗
(以上内容均参考自美国FDA官网BRIUMVI说明书英文版 2022.12)
1.如果您发现该药品信息有任何错误,请联系我们修改,我们将热忱感谢您的批评指正!
2.本站所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考!
