





奥普杜拉格(Opdualag)是黑色素瘤的双免疫疗法,是一个同类首创(first-in-class)的双免疫联合固定剂量复方制剂。
 美国施贵宝
美国施贵宝
适用于12岁以上不可切除或转移性黑色素瘤的成人和儿童患者的治疗
(1)成人患者和体重至少40 kg的12岁或以上儿童患者的本药推荐剂量为每4周静脉滴注480mg纳武利尤单抗和160mg瑞拉利单抗,直至疾病进展或出现不可接受的毒性
(2)12岁或以上体重小于40公斤的儿科患者的推荐剂量尚未确定
不建议减少本品的剂量
一般来说,对于严重的(3级)免疫介导的不良反应(IMARs),暂停使用本品,对于危及生命的(4级)IMARs,需要全身免疫抑制治疗的复发性严重(3级)IMARs,或在开始使用类固醇的12周内无法将皮质类固醇剂量减少到每天10毫克或更少的泼尼松或同等剂量,则永久停用本品
表1总结了对需要处理的不良反应的剂量修改:

本品是纳武利尤单抗和瑞拉利单抗的固定剂量组合,在给药前,目视检查药品瓶中的溶液是否有颗粒物质和变色,本品为透明至乳白色,无色至微黄色溶液,如果溶液混浊、变色或含有除一些半透明或白色颗粒外的外来颗粒物质,则丢弃小瓶
(1)准备
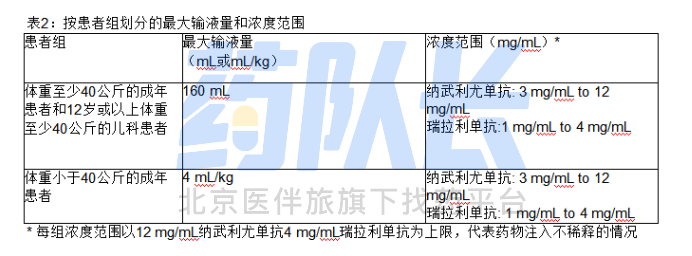
①在输液溶液的制备过程中,使用无菌技术以确保无菌,因为产品不含防腐剂,本品可以稀释或未稀释给药,并按下表2规定的最终浓度给药
②取出所需量的本药并转移到静脉注射容器中
③本品与邻苯二甲酸二(2-乙基己基)酯(DEHP)-增塑型聚氯乙烯(PVC),乙酸乙酯(EVA)和聚烯烃(PO)静脉注射袋兼容
④如果在给药前稀释本品:用0.9%氯化钠注射液(USP)或5%葡萄糖注射液(USP)稀释本药溶液,配制出符合下表2规定的最终浓度和最大输注量参数的输注液,然后将稀释后的溶液轻轻倒置混合
⑤不要摇晃,输液准备后,丢弃部分用过的小瓶或空小瓶
(2)配制溶液的储存
储存配制好的溶液:从制备时间到注射结束,在室温和室内光照下放置不超过8小时,配制后的溶液如在配制后8小时内未使用,应丢弃;或者在2°C至8°C的冷藏条件下,从制备时起不超过24小时的避光保护,包括将输液袋平衡到室温的时间和输液的持续时间,如果配制后24小时内未使用,应丢弃配制好的溶液,不要冷冻溶液
(3)管理
通过含有无菌,无热原,低蛋白结合的在线聚醚砜(PES),尼龙或聚偏氟乙烯(PVDF)过滤器(孔径为0.2微米至1.2微米)的静脉注射线进行输液30分钟以上,在输注结束时冲洗静脉导管,不要在同一静脉管道中同时使用其他药物
最常见的不良反应(≥20%)是肌肉骨骼疼痛、疲劳、皮疹、瘙痒和腹泻
最常见的实验室异常(≥20%)是血红蛋白降低、淋巴细胞减少、转氨酶升高和钠降低
尚未明确
在原纸箱中冷藏(2°C至8°C),避光,不要冷冻或摇晃
12岁以上患者
尚未明确
24个月
注射剂
美国施贵宝
本品主要有效成分为:纳武利尤单抗和瑞拉利单抗
注射剂:每20毫升有240 mg纳武利尤单抗和80 mg瑞拉利单抗(每毫升12 mg和4 mg),为透明至乳白色、无色至微黄色溶液,单剂量瓶
(1)可能破坏外周耐受性,并诱导免疫介导的不良反应(IMARs)
(2)早期识别和管理IMARs对于确保安全使用至关重要,密切监测患者是否有可能是影响IMARs的临床表现的症状和体征
(3)在基线时和治疗期间定期评估肝酶、肌酐和甲状腺功能,对于疑似IMARs的病例,开始适当的检查,以排除其他病因,包括感染,及时进行医疗管理,包括适当的专业咨询
(4)根据严重程度停用或永久停用,一般来说,如果需要中断或停用,给予全身皮质类固醇治疗(1-2mg/kg/天的强的松),直到不良反应改善到1级或更少,开始皮质类固醇减量,并继续减少至少1个月,考虑使用其他全身药物
严重或危及生命的输注相关反应停止严重或减缓有轻度或中度输注相关反应的患者的输注速率
(1)在接受异基因造血干细胞移植(HSCT)的患者接受PD1/PD-L1受体阻断抗体治疗之前或之后,可能发生致命和其他严重并发症
(2)密切随访患者,寻找移植相关并发症的证据,并及时进行干预
(3)考虑在异体HSCT之前或之后使用PD1/PD-L1受体阻断抗体治疗的益处和风险
基于其作用机制和数据研究,本品可以导致胎儿伤害,建议具有生殖潜力的女性在最后一剂治疗后至少5个月使用有效避孕
(以上参考自FDA美国药监局英文说明书2022.03版)
1.如果您发现该药品信息有任何错误,请联系我们修改,我们将热忱感谢您的批评指正!
2.本站所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考!
