

适用于治疗经 CFDA 批准的检测方法确定的 BRAF V600 突变阳性的不可切除或转移性黑色素瘤
(1)患者必须经由CFDA批准的检测方法确定的证明肿瘤为BRAF V600 突变阳性,才可使用维莫非尼治疗
(2)维莫非尼不能用于BRAF野生型黑色素瘤患者
(3)首剂药物应在上午服用,第二剂应在此后约 12 小时,即晚上服用,每次服药均可随餐或空腹服用
(4)用一杯水送服药物,服药时整片吞下维莫非尼片剂,不应咀嚼或碾碎片剂
(1)推荐剂量为:960 mg(四片 240 mg 片剂),每日两次
(2)治疗持续时间:建议维莫非尼治疗应持续至疾病进展或发生不可接受的毒性反应
(3)漏服:如果漏服一剂计划的药物,可在下一剂服药 4 小时以前补服漏服的药物,以维持每日两次的给药方案,不应同时服用两剂药物
(4)呕吐:如果维莫非尼服药后发生呕吐,患者不应追加剂量,而应按常规剂量继续治疗
(1)对于伴有症状的不良事件或QTc间期延长的处理,可能需要按照表 1 或表 2 降低剂量、 暂时中断用药或停止维莫非尼治疗
(2)对于出现皮肤鳞状细胞癌(cuSCC)等不良反应,不建议调整剂量或中断用药
(3)不建议采用低于480 mg每日两次的剂量
表1:基于不良反应的剂量调整方案
| 毒性级别(CTC-AE)a | 建议的剂量调整方案 |
| 1 级或 2 级(可耐受) | 维持维莫非尼960mg,每日两次 |
| 2 级(不可耐受)或 3 级 | |
| 第 1 次出现(不可耐受)2 级或 3 级 AE | 暂时中断治疗,直至不良事件恢复至 0-1 级。恢复用药时给药剂量 为 720mg,每日两次 (如果之前已经降低过剂量,恢复给药剂量 为 480mg,每日两次) |
| 第 2 次出现(不可耐受)2 级或 3 级 AE,或治疗中断后未缓解 | 暂时中断治疗,直至不良事件恢复至 0-1 级。恢复用药时给药剂量 为 480mg,每日两次(如果之前剂量已经降低到 480mg,每日两 次,永久性停药) |
| 第 3 次出现(不可耐受)2 级或 3 级 AE,或治疗中断后未缓解 | 永久性停药 |
| 4 级 | |
| 第 1 次出现任何 4 级 AE | 永久性停药或暂时中断治疗,直至不良事件恢复至 0-1 级。恢复用 药时给药剂量为 480mg,每日两次(如果之前剂量已经降低到 480mg,每日两次,永久性停药) |
| 第 2 次出现任何 4 级 AE | 永久性停药 |
a 临床不良事件的强度根据不良事件常见术语标准(CTC-AE)4.0版进行评级
表2:基于QT间期延长的剂量调整方案
| QTc值 | 推荐剂量调整方案 |
| 基线时QTc > 500 ms | 不建议开始服用该药 |
| QTc延长同时满足QTc>500 ms和相对于治疗前的变化值> 60 ms | 永久性停药 |
| 治疗期间第1次发生QTc>500ms,且QTc相对于治疗前的变化值≤ 60 ms | 暂时中断治疗,直至QTc降至500 ms以下参见【注意事项】中的监测指标恢复用药时给药剂量为720mg,每日两次 (如果之前 已经降低过剂量,恢复给药剂量为480mg,每日两次) |
| 治疗期间第2次发生QTc>500 ms,且QTc相对于治疗前的变化值≤ 60 ms | 暂时中断治疗,直至QTc下降至500 ms以下参见【注意事项】中的监测指标恢复用药时给药剂量为480mg,每日两次(如果之前剂 量已经降低到480mg,每日两次,永久性停药) |
| 治疗期间第3次发生QTc>500 ms,且QTc相对于治疗前的变化值≤ 60 ms | 永久性停药 |
(1)儿童:维莫非尼对18 岁以下患者的安全性和有效性尚未确立,维莫非尼未批准用于18 岁以下的患者
(2)老年人:对于年龄≥65岁的患者,无特殊剂量调整需求
(3)肾功能受损:对于轻度或中度肾功能受损的患者,无需进行起始剂量调整;对于重度肾功能受损的患者,由于数据不足,无法确定是否需要进行剂量调整
(4)肝功能受损:对于轻度或中度肝功能受损的患者,无需进行起始剂量调整;对于重度肝功能受损的患者,由于数据不足,无法确定是否需要进行剂量调整
1.最常见(每个试验中≥30%)的各种级别不良反应:关节痛、皮疹、脱发、疲劳、光敏反应、恶心、瘙痒和皮肤乳头状瘤和皮肤角化症
2.最常见(≥5%)3级不良反应:皮肤鳞状细胞癌、角化棘皮瘤、皮疹、关节痛和γ-谷氨酰转移酶(GGT)升高
禁用于已知对维莫非尼或本品任何辅料过敏的患者
遮光,密封,干燥处,30℃以下保存
成人
(1)维莫非尼是一种中度 CYP1A2 抑制剂和 CYP3A4 诱导剂,维莫非尼可升高主要经 CYP1A2 代谢药物的血药浓度,并降低主要经 CYP3A4 代谢药物的血药浓度,不建议维莫非尼与治疗窗口较窄的药物(通过 CYP1A2 和 CYP3A4 代谢)联合用药,如果有临床指征,可以考虑减小合并 CYP1A2 底物的剂量
(2)在维莫非尼与华法林联合用药的情况下,应谨慎,并考虑附加 INR(国际标准化比值)监测, 维莫非尼是流出转运蛋白 P-糖蛋白(P-gp)的一种抑制剂,维莫非尼可升高 P-gp 底物药物的血药浓度,维莫非尼与 P-gp 底物同时用药时,应谨慎,如果出现临床指征,可考虑减小合并 P-gp 底物药物的剂量
维莫非尼是 CYP3A4 的一种底物,因此,与强效 CYP3A4 抑制剂或诱导剂的联合应用 可改变维莫非尼的浓度,在联合给予维莫非尼与强效 CYP3A4 抑制剂和诱导剂的情况下, 应谨慎,在与强效 CYP3A4 抑制剂联合给药期间,如果存在临床指征,则可考虑减低维莫非尼的剂量
36 个月
片剂
瑞士罗氏
本品主要成分:维莫非尼
化学结构式为:
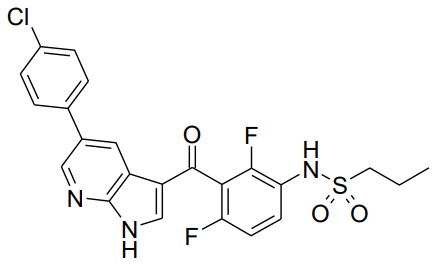
两面凸起、粉白色至橙白色的薄膜衣片
皮肤鳞状细胞癌病例通常采用简单切除加以 处理,且患者能够继续治疗,不需要剂量调整
患者应接受头部和颈部检查,其中应包含治疗开始前的至少一次口腔粘膜视诊和淋巴结触诊,并在治疗期间每3个月检查一次
在临床试验中,已报道新发原发性黑色素瘤,病例的处理方式为切除,患者继续接受治疗,而不需要调整剂量,应根据以上针对皮肤鳞状细胞癌的原则对皮肤病变进行监测
基于其作用机制,维莫非尼可引起与 RAS 突变相关的癌症进展, 对于既往发生或合并发生 RAS 突变相关癌症的患者,应谨慎使用维莫非尼
维莫非尼不能用于BRAF 野生型黑色素瘤患者
患者在胰腺炎发作后,若重新接受维莫非尼治疗,应对其进行密切监测
重度超敏反应包括:全身性皮疹和红斑或低血压,对于发生重度超敏反应的患者,应永久性停止维莫非尼治疗
对于发生重度皮肤反应的患者,应永久性停止维莫非尼治疗
在同步或按顺序给予放射治疗时,应谨慎使用维莫非尼
对于存在无法纠正的电解质异常、长QT综合征或正在服用已知能延长QT间期的药物的患者,不建议采用维莫非尼治疗
在开始治疗之前,应监测肝酶水平(转氨酶和碱性磷酸酶)和胆红素水平,在治疗过程中,应每月监测一次, 或根据临床需要确定监测频率,对于实验室异常,应酌情采用减量、治疗中断或停止治疗的方式加以处理
建议所有患者在服用维莫非尼期间避免日光暴露,在服用药物期间,应建议患者穿戴防护性服装,并在室外使用广谱 UVA/UVB 防晒霜和润唇膏(SPF≥ 30),有助于在日晒环境下保护患者,对于 2 级(不可耐受)或更高级别不良事件的光敏反应,建议调整剂量
对于掌腱膜挛缩症和足跖筋膜纤维瘤不良反应,应酌情采用减量、中断治疗或停止治疗的方式处理
已报告的严重眼部反应包括葡萄膜炎,应定期监测患者是否发生某些眼部不良反应
不建议 ipilimumab 与维莫非尼联合用药
(以上内容参考自维罗非尼中文版说明书2022.02版)
1.如果您发现该药品信息有任何错误,请联系我们修改,我们将热忱感谢您的批评指正!
2.本站所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考!
