





XACDURO是将一种较老的抗生素舒巴坦和一种新抗生素杜洛巴坦配对使用, 旨在治疗鲍曼不动杆菌引起的感染。
 美国ENTASIS
美国ENTASIS
1.适应症
医院获得性细菌性肺炎和呼吸机相关细菌性肺炎(HABP/VABP)XACDURO 适用于 18 岁及以上患者,用于治疗由鲍曼不动杆菌-炭疽杆菌复合体易感分离株引起的医院获得性细菌性肺炎和呼吸机相关细菌性肺炎(HABP/VABP)
2.使用限制
XACDURO不适用于除鲍曼不动杆菌-炭疽杆菌复合体易感分离株外的病原体引起的HABP/VABP
3.使用方法
为减少耐药菌的产生并保持 XACDURO和其他抗菌药物的疗效,XACDURO 只能用于治疗或预防已证实或强烈怀疑由易感细菌引起的感染,如果可以获得培养和药敏信息,在选择或调整抗菌治疗时应加以考虑,在缺乏此类数据的情况下,当地的流行病学和易感性模式可能有助于根据经验选择治疗方法
XACDURO 是一种联合包装产品,含有注射用舒巴坦和注射用杜鲁巴坦
(1)对于肌酐清除率(CLcr)为 45 至 129 ml/分钟的成人,XACDURO 的推荐剂量为每 6 小时静脉注射 1 g舒巴坦和 1 g杜洛巴坦,持续 3 小时
(2)建议对 CLcr 低于 45 ml/分钟和 CLcr 大于或等于 130 ml/分钟的患者调整 XACDURO 的给药方案
(3)建议使用 XACDURO 的疗程为 7 至 14 天,治疗持续时间应根据患者的临床状况而定
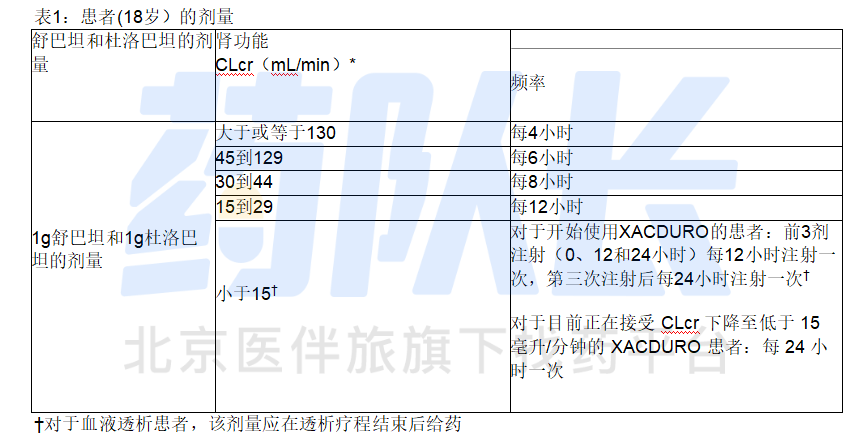
(1)基于肾功能的 XACDURO 在 18 岁及以上患者中的推荐剂量见表 1
(2)建议调整肌酐清除率(CLcr)小于 45 ml/分钟的患者和肾脏清除率增高(CLcr 大于或等于 130 ml/分钟)的患者的给药方案
(3)对于接受间歇性血液透析(HD)的患者,应在完成 HD 后立即开始服用 XACDURO
(4)对于肾功能波动的患者,应监测 CLcr 并相应调整剂量
在输注给患者之前,应将配制好的 XACDURO 溶液置于室温下(15 至 30 分钟),通过静脉注射(IV)在 3 小时内输注足量的 XACDURO
(1)XACDURO 是一种共同包装的试剂盒,内含 1 个透明的单剂量舒巴坦 1g 瓶和 2 个琥珀色的单剂量杜洛巴坦 0.5g 瓶,均为无菌粉末,在静脉输注前必须用无菌技术重新配制和进一步稀释
(2)XACDURO 不含抑菌防腐剂,配制好的溶液必须在 2°C 至 8°C (36°F 至 46°F)的冷藏条件下储存 24 小时内使用,未用完的溶液应丢弃
(3)配制 XACDURO 所需的物品:
①XACDURO 试剂盒(包括一个舒巴坦 1 克单剂小瓶和两个舒巴坦 0.5 克单剂小瓶)
②100 mL 输液袋,内含 0.9% 氯化钠注射液,USP10 mL 无菌注射用水
③10 mL 无菌注射器和酒精擦拭布
(1)用 5 mL 无菌注射用水调配 1 g 舒巴坦单剂量瓶,轻轻摇动使其溶解,每个重组瓶中每 5 mlof 的无色至微黄色透明溶液含有 1 g 舒巴坦,重组溶液不能直接注射,必须在静脉注射前稀释
(2)用 2.5 毫升注射用无菌水稀释每个 0.5 克的杜洛巴坦单剂量瓶,并轻轻摇动使其溶解
(3)每个重组瓶中每 2.5 mL 淡黄色至橙色的澄清溶液含有 0.5 g 杜洛巴坦,重组溶液不可直接注射,必须在静脉注射前稀释,
(4)为了配制所需的 XACDURO 剂量,抽取 5 毫升重组舒巴坦和毫升(每瓶 2.5 毫升)重组杜洛巴坦,将提取的舒巴坦和杜洛巴坦体积加入 100 毫升注射用 0.9% 氯化钠(USP)输液袋中,丢弃未使用的部分
(5)在溶液和容器允许的情况下,给药前应目测肠外用药产品是否有颗粒物和变色,配制好的 XACDURO 溶液应为无颗粒的淡黄色至橙色透明溶液,如果 XACDURO 溶液浑浊或含有微粒,请勿施用
XACDURO与0.9%氯化钠注射液(USP)兼容,XACDURO与含有其他药物或其他稀释剂的溶液的配伍性尚未确定,XACDURO不应与其他药物混合或物理添加到含有其他药物的溶液中
将准备好的袋子存放在2°C至8°C(36°F至46°F)的冰箱中,直到给药,从粉末开始重构到输注结束的时间不应超过24小时,不要冻住
最常见的不良反应(发生率>10%)是肝检查异常、腹泻、贫血和低钾血症
对 XACDURO 的成分(舒巴坦和杜鲁巴坦)或其他 beta-内酰胺类抗菌药有严重过敏史的患者禁用 XACDURO
2-8℃冷藏保存,不要冷冻
成人。孕妇、老人请在医生指导下使用。
有机阴离子转运体 1 (OAT1) 抑制剂同时服用 OAT1 抑制剂可能会增加舒巴坦的血浆浓度,不建议在服用 XACDURO 的同时服用 OAT1 抑制剂(如丙磺舒)
24个月
注射剂
美国ENTASIS
本品主要有效成分为舒巴坦和杜洛巴坦
其化学结构如下:
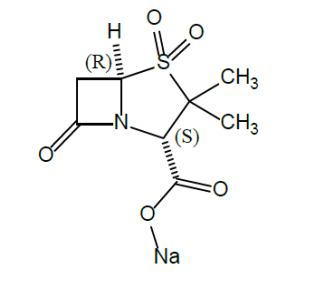
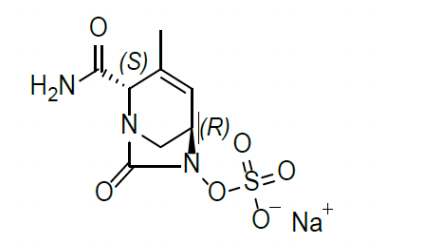
XACDURO是一种共包装试剂盒,包含以下两种成分作为无菌粉末用于重组:1个透明单剂量注射用舒巴坦1g(白色至灰白色粉末);2个琥珀色注射用杜氯巴坦0.5g(固体饼状或粉末状)
在接受β-内酰胺类抗菌药物治疗的患者中,偶尔会出现严重的致命超敏反应 (过敏反应)和严重的皮肤反应, 在开始使用 XACDURO 治疗前,应仔细询问以前对碳青霉烯类、青霉素类、头孢菌素类、其他 β-内酰胺类和其他过敏原的过敏反应,如果出现过敏反应,请停用 XACDURO
(1)难辨梭状芽胞杆菌相关性腹泻(CDAD)在使用几乎所有抗菌剂(包括XACDURO)时均有报道,其严重程度从轻度腹泻到致命性结肠炎不等
(2)所有使用抗菌药物后出现腹泻的患者都必须考虑CDAD
(3)如果怀疑或确认CDAD,应评估继续使用XACDURO治疗的风险/获益,给予适当的液体和电解质管理、蛋白质补充、艰难梭菌抗菌药物治疗和手术评估应根据临床指征建立
在没有证实或强烈怀疑细菌感染或预防指征的情况下开XACDURO不太可能给患者带来益处,并会增加耐药细菌发展的风险
(以上参考自FDA美国药监局英文说明书2023.07版)
1.如果您发现该药品信息有任何错误,请联系我们修改,我们将热忱感谢您的批评指正!
2.本站所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考!
