


用于治疗局部晚期或转移性尿路上皮癌(mUC)的成年患者,这些患者有需满足:
1.易感FGFR3或FGFR2基因改变
2.既往至少一次含铂化疗期间或之后病情进展(包括新辅助或辅助含铂化疗12个月内)
根据FDA批准的配套诊断仪检测到的肿瘤标本中存在的易感性FGFR基因改变,来选择患者使用本药治疗局部晚期或转移性尿路上皮癌
(1)推荐起始剂量为8mg(两片4mg片),每日口服一次,根据血清磷酸盐(PO4)水平和14至21天的耐受性,剂量增加至9mg(三片3mg片),每日一次
(2)整片吞下,伴随或不伴随食物,如果服用本药后任何时间出现呕吐,应在第二天服用下一剂
(3)治疗应持续至疾病出现进展或发生不可接受的毒性
(1)根据血清磷酸盐水平增加剂量
开始治疗后14 - 21天评估血清磷酸盐水平,如果血清磷酸盐水平< 5.5 mg/dL且无眼部疾病或2级或更大不良反应,则增加剂量至9 mg每天,每日1次,并且每月监测磷酸盐水平以防高磷血症
(2)根据不良反应调整剂量
表1:剂量减少计划
一次的剂量 | 第一次剂量 减少 | 第二次剂量 减少 | 第三次剂量 减少 | 第四次剂量 减少 | 第五次剂量 减少 |
9 mg(三份3 mg药片 | 8 mg(两个4毫克药片 | 6 mg(两个3毫克药片 | 5毫克(一片5毫克药片) | 4 mg(一份4毫克 药片 | 停药 |
8mg(2片4mg) | 6 mg(两个3毫克药片) | 5毫克(一片5毫克药片) | 4毫克(1片4毫克) | 停药 | |
表2:针对不同不良反应的建议剂量调整
不良反应 | 剂量修改 |
高磷血症 | |
所有患者应将磷酸盐的摄入量限制在每天600-800mg,如果血清磷酸盐水平高于7.0 mg/dL,请考虑添加口服磷酸盐结合剂,直到血清磷酸盐水平恢复到<5.5 mg/dL | |
5.6-6.95 mg/dL (1.8-2.3 mmol/L ) | 继续服用当前剂量。 |
7.0-9.07 mg/dL (2.3-2.9mmol/L ) | 暂停用药,每周重新评估,直到水平恢复到< 5.5 mg/dL(或基线),然后以相同的剂量水平重新服药。对于持续>1周的高磷血症,可减少剂量 |
> 9.0 mg/dL ( > 2.9 mmol/L ) | 暂停用药,每周重新评估,直到水平恢复到< 5.5 mg/dL(或基线),然后可以降低1个剂量水平(参考表1)恢复用药 |
> 10.0 mg/dL(>3.2mmol/L) 或基线肾功能显著改变 或3级高钙血症 | 保留平衡,每周重新评估,直到水平恢复到< 5.5 mg/dL(或基线),然后可以降低2个剂量水平(参考表1)恢复用药 |
中枢性浆液性视网膜病变/视网膜色素上皮脱离(CSR/RPED) | |
1级:无症状;仅需进行临床或诊断性观察 | 暂停用药直至该症状恢复。如果在4周内解决,可以降低1个剂量水平(参考表1)恢复用药,如果一个月没有复发,请考虑增加剂量。如果连续2次眼科检查结果稳定,但没有恢复迹象,则按下一个较低的剂量水平恢复剂量 |
2级:视力20/40或以上或较基线时视力水平下降≤3行(视力表) | 暂停用药直至该症状恢复。如果在4周内解决,可以降低1个剂量水平(参考表1)恢复用药 |
3级:视力20/40以下或较基线时视力水平下降﹥3行(视力表) | 暂停用药直至该症状恢复。如果在4周内解决,可以降低2个剂量水平(参考表1)恢复用药,如果复发,请考虑永久停药 |
4级:患眼的视力为20/200或出现更差的眼部反应 | 永久停药 |
其他的不良反应 a | |
3级 | 暂停用药直至该症状恢复到1级或基线,恢复较低的剂量水平 |
4级 | 永久停药 |
a:使用美国国家癌症研究所不良事件通用术语标准(NCI CTCAEv4.03)进行剂量调整分级
最常见的不良反应包括实验室异常(≥20%)为磷酸盐升高、口炎、疲劳、肌酐升高、腹泻、口干、指甲紊乱、丙氨酸转氨酶升高、碱性磷酸酶升高、钠降低、食欲下降、白蛋白降低、味觉障碍、血红蛋白降低、皮肤干燥、天门冬氨酸转氨酶升高、镁降低、干眼、脱发、足底红肿综合征、便秘、磷酸盐减少,腹痛,钙增加,恶心,肌肉骨骼疼痛
尚不明确
遮光,密封,干燥处保存
成人
中度CYP2C9或强CYP3A4抑制剂 | |
临床影响 | 与中度CYP2C9或强CYP3A4抑制剂联合给药增加了阿达非替尼的血浆浓度,血浆浓度的增加可能导致药物毒性增加
|
临床管理 | 在使用其他药物治疗期间,考虑非中度CYP2C9或强CYP3A4抑制剂的替代疗法 如果不可避免地要联合使用中度CYP2C9或强CYP3A4抑制剂,请密切监测不良反应,并考虑相应的剂量调整 如果停用中度CYP2C9或强CYP3A4抑制剂后,没有发生药物相关毒性的情况下,可以增加剂量 |
强CYP2C9或CYP3A4诱导剂 | |
临床影响 | 与CYP2C9或CYP3A4的强诱导剂共同使用可显著降低本药的血浆浓度,导致降低疗效 |
临床管理 | 避免与CYP2C9或CYP3A4强诱导剂同时使用 |
中度CYP2C9或CYP3A4诱导剂 | |
临床影响 | 与CYP2C9或CYP3A4的强诱导剂共同使用可显著降低本药的血浆浓度,导致降低疗效 |
临床管理 | (1)如果在治疗开始时必须同时使用中度CYP2C9或CYP3A4诱导剂,则按照推荐剂量使用本药(每日8毫克,根据第14至21天的血清磷酸盐水平和耐受性,可能增加到9毫克每日一次) (2)如果根据血清磷酸盐水平和耐受性,在初始剂量增加期后必须同时给药中等CYP2C9或CYP3A4诱导剂,则将本药的剂量增加至9 mg (3)当CYP2C9或CYP3A4的中等诱导剂被停用时,在没有药物相关毒性发生的情况下,继续以相同的剂量进行治疗 |
血清磷酸盐水平改变剂 | |
临床影响 | 与其他血清磷酸盐水平改变剂联合使用可能会增加或降低血清磷酸盐水平,由于血清磷酸盐水平改变剂(厄达替尼除外)引起的血清磷酸盐水平的变化可能会干扰根据血清磷酸盐水平确定初始剂量增加所需的血清磷酸盐水平 |
临床管理 | 在根据血清磷酸盐水平(第14至21天)之前,避免与本药共同使用血清磷酸盐水平改变药物 |
CYP3A4底物 | |
临床影响 | 与CYP3A4底物共同给药可能会改变CYP3A4底物的血浆浓度,改变CYP3A4底物的血浆浓度可能导致CYP3A4底物的活性丧失或毒性增加 |
临床管理 | 避免与CYP3A4敏感底物共同给药 |
OCT2底物 | |
临床影响 | 与OCT2底物共同给药可能会增加OCT2底物的血浆浓度,OCT2底物的血浆浓度升高可能导致OCT2底物的毒性增加 |
临床管理 | 考虑非OCT2底物的替代疗法,或考虑根据耐受性减少OCT2底物(如二甲双胍)的剂量 |
P-糖蛋白(P-gp)底物 | |
临床影响 | 与P-gp底物共同使用可能会增加P-gp底物的血浆浓度,P-gp底物血浆浓度升高可能导致P-gp底物毒性增加 |
临床管理 |
|
24个月
片剂
美国强生
本品主要有效成分为厄达替尼
其化学结构如下:
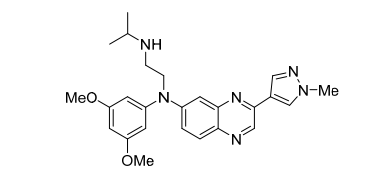
3 mg:黄色,圆形双凸,涂膜,一面涂有“3”;另一面是“EF” ;4mg:橙色,圆形双凸,镀膜,一边去掉“4”;另一边是“EF” ;5mg:棕色,圆形双凸,薄膜包膜,一面有“5”;另一边是“EF”
(1)本品可引起眼部疾病,包括中枢浆液性视网膜病变/视网膜色素上皮脱离(CSR/RPED),导致视野缺损,所有患者均应根据需要使用眼镇痛药进行干眼预防
(2)治疗前4个月每月进行一次眼科检查,治疗后每3个月进行一次眼科检查,并随时紧急检查视力症状
(3)眼科检查应包括视力评估、裂隙灯检查、眼底镜检查和光学相干断层扫描
(4)当发生中枢浆液性视网膜病变(CSR)时应停用本药,如果在4周内没有解决或严重程度为4级,则永久停药,对于眼部不良反应,遵循剂量调整指南
(1)本品可引起高磷血症,导致软组织矿化、皮肤钙质沉着、非尿毒症性钙过敏症和血管钙化
(2)在整个治疗过程中监测高磷血症,所有患者应将磷酸盐摄入量限制在每天600-800毫克,如果血清磷酸盐高于7.0 mg/dL,可以考虑添加口服磷酸盐结合剂,直到血清磷酸盐水平恢复到<5.5 mg/dL
(3)根据高磷血症的持续时间和严重程度,根据表2暂停、减少或永久停用本药
(1)根据作用机制和动物生殖研究的结果,本药给药给孕妇时可造成胎儿伤害
(2)应告知孕妇对胎儿的潜在风险,建议有生育潜力的女性患者在使用本药治疗期间和最后一次给药后一个月内使用有效的避孕措施
(3)建议有生育潜力的女性伴侣的男性患者在本药治疗期间和最后一次给药后一个月内使用有效的避孕措施
(以上参考自FDA美国药监局英文说明书2023.03版)
1.如果您发现该药品信息有任何错误,请联系我们修改,我们将热忱感谢您的批评指正!
2.本站所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考!
