



是一种CD20指导的细胞溶解抗体,用于先前未治疗的II期大体积,III或IV滤泡性淋巴瘤的治疗。
 瑞士罗氏
瑞士罗氏
本品与氯霉素联合用于治疗以前未治疗的慢性淋巴细胞白血病患者。
(1)本品与苯达莫司汀联合,随后进行本品单药治疗,适用于利妥昔单抗治疗后复发或难治性滤泡性淋巴瘤患者。
(2)本品联合化疗后再单药治疗至少达到部分缓解的患者,适用于先前未治疗的II期、III期或IV期大体积滤泡性淋巴瘤的成人患者。
(1)每次输液前预先用药。
(2)对肿瘤溶解综合征高危患者给予预防性水合和抗高尿酸药。
(3)只能通过专用管道静脉输注给药。
(4)不要给药静脉推或栓剂给药。
(5)定期监测血液计数。
(6)本品只能由医护人员在适当的医疗支持下使用,以控制严重的输液相关反应,这些反应一旦发生可能致命。
表1 慢性淋巴细胞白血病患者的6个28天治疗周期中给予本品的剂量
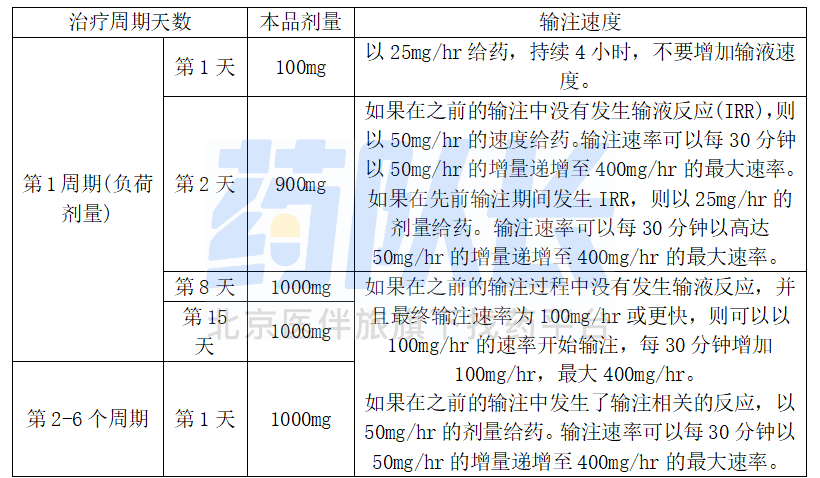
如果错过了本品的计划剂量,应尽快进行错过的剂量,并调整给药计划以保持两次给药之间的时间间隔,如果合适,没有完成第1天周期1剂量的患者可以继续进行第2天周期1剂量。
(1)本品每剂量为1000mg静脉给药见表2,。
(2)对于复发或难治性滤泡性淋巴瘤患者,本品联合苯达莫司汀以6个28天的周期给药,在最初的6个周期中病情稳定、完全缓解或部分缓解的患者应继续使用本品1000mg单药治疗,最长可达2年。
(3)对于先前未治疗的滤泡性淋巴瘤患者,给予本品和以下化疗方案之一:
①6个28天周期联合苯达莫司汀。
②6个21天周期联合CHOP,随后2个额外的21天周期单独给予本品。
③8个21天周期联合CVP.
(4)先前未治疗的滤泡性淋巴瘤患者在最初的6或8个周期中达到完全缓解或部分缓解,应继续使用本品1000mg单药治疗,最长可达2年。
(5)本品应在第1周期以标准输注速率给药(见表2),对于在第1周期中没有经历3级或更高IRR的滤泡性淋巴瘤患者,本品可以从第2周期开始以较短的约90分钟输注的方式给药(见表3),并继续预用药。
表2 滤泡性淋巴瘤患者在6-8个治疗周期内给予本品的剂量和标准输注速率,随后进行本品单药治疗。
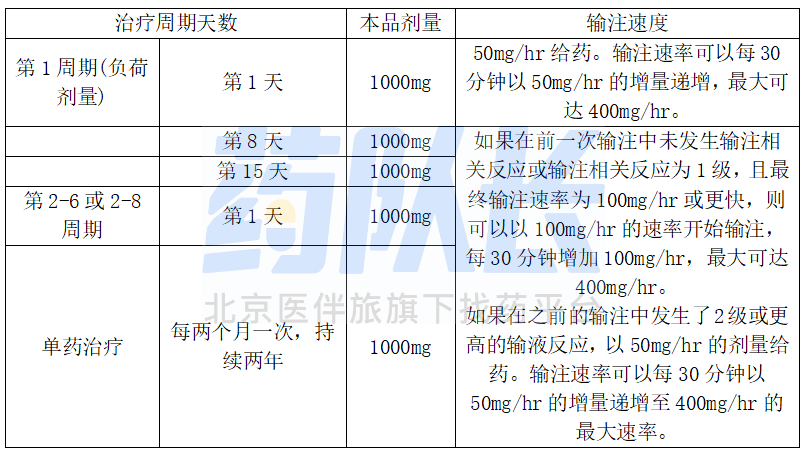
表3 输注本品治疗滤泡性淋巴瘤患者90分钟的剂量和输注速率
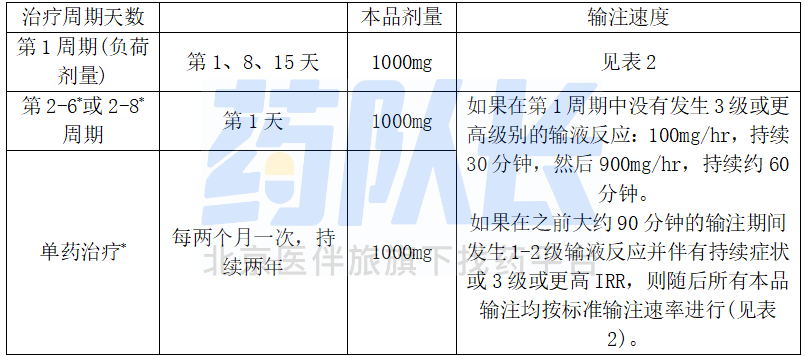
*考虑在第1周期及后续周期中对本品未发生3级或以上输注相关反应的滤泡性淋巴瘤患者输注约90分钟。
(6)如果错过了本品的计划剂量,应尽快补足,在使用本品和化疗期间,相应调整给药计划,保持化疗周期之间的时间间隔,在单药治疗期间,后续给药保持原给药计划,在诱导期最后一次给药后大约两个月开始单药治疗。
静脉输注本品时可能出现低血压,考虑在每次输注本品前后12小时以及给药后1小时不进行降压治疗。
表4 输注本品前用药减少输注相关反应
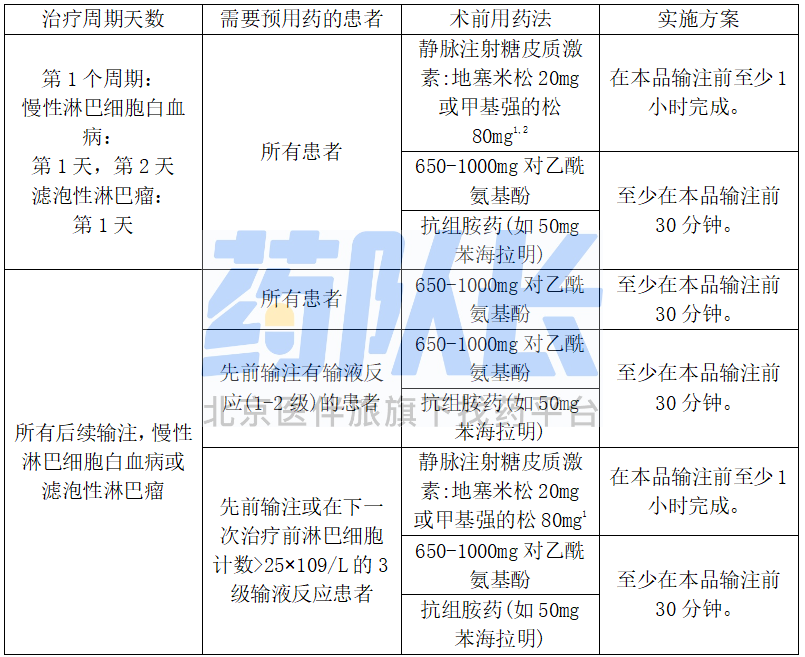
预用药适用于标准和大约90分钟的输液。
1不推荐使用氢化可的松,因为它在降低输液反应发生率方面没有效果。
2如果在本品的同一天给予含糖皮质激素的化疗方案,如果在本品前至少1小时给予糖皮质激素,可以作为口服药物给药,在这种情况下,不需要额外的静脉注射糖皮质激素作为用药前。
高肿瘤负荷、高循环绝对淋巴细胞计数(大于25×109/L)或肾功能损害的患者被认为有肿瘤溶解综合征的危险,应接受预防,预先使用抗高尿酸药(如别嘌呤醇或拉布立酶),并确保在本品治疗开始前充分补水,根据需要,在每次后续输注本品之前继续进行预防。
3级至4级中性粒细胞减少持续超过一周的患者强烈建议接受抗微生物预防治疗,直到中性粒细胞减少缓解至1级或2级,对于严重和持续时间(>1周)的中性粒细胞减少患者,考虑抗病毒和抗真菌预防。
如果患者出现输液反应,请按以下方法调整输液:
①4级(危及生命):立即停止输注并永久停用本品。
②3级(严重):中断输液并控制症状。
1)对于在标准输注过程中出现3级输液反应的患者,在症状缓解后,考虑重新开始本品输注,不超过先前速率的一半(发生输液反应反应时使用的速率),如果患者没有出现任何进一步的输液反应症状,输注速率升高可以根据治疗周期剂量的适当增量和间隔恢复,如果患者在再次挑战时出现3级或更高的输液反应,则永久停止治疗。
2)对于在大约90分钟的输注过程中出现3级输液反应的滤泡性淋巴瘤患者,在症状缓解后,可以以不超过先前输注速率的一半(发生输液反应时使用的速率)重新开始输注,且不大于400mg/hr,按标准速率进行后续输液,如果患者在再次给药时出现3级或更高的输液反应,则永久停止治疗。
仅对于慢性淋巴细胞白血病患者,第1天输注速率可在1小时后增加至25mg/hr,但不能进一步增加。
③1-2级(轻度至中度):降低输液速度或中断输液并控制症状。在症状缓解后,继续或恢复本品输注,如果患者没有出现任何进一步的输液反应症状,输注速率可根据治疗周期剂量以适当的增量和间隔恢复上升,仅对于慢性淋巴细胞白血病患者,第1天输注速率可在1小时后增加至25mg/hr,但不能进一步增加。
如果患者出现感染,3级或4级细胞减少,或2级或更高的非血液学毒性,可考虑中断治疗。
最常见的不良反应(发生率≥20%和≥2%)为:
1.先前未治疗的慢性淋巴细胞白血病:输注相关反应和中性粒细胞减少。
2.复发或难治性非霍奇金淋巴瘤:输注相关反应、疲劳、中性粒细胞减少、咳嗽、上呼吸道感染和肌肉骨骼疼痛。
3.既往未治疗的非霍奇金淋巴瘤:输注相关反应、中性粒细胞减少、上呼吸道感染、咳嗽、便秘和腹泻。
本品禁用于已知对本品或任何辅料有超敏反应(如过敏反应)的患者,或既往使用过本品的血清疾病患者。
储存在在2°C至8°C。不要使用超出纸盒上标记失效日期。本品小瓶应被避光保护。 请勿冻结。请勿摇动。
成人患者。孕妇、老人及儿童请在医师指导下使用。
尚未明确。
36个月
注射剂
瑞士罗氏
本品的主要成分是Obinutuzumab。
本品为透明,无色至微棕色溶液。
使用抗CD20抗体(如GAZYVA)治疗的患者可能发生乙型肝炎病毒(HBV)再激活,在某些情况下导致暴发性肝炎、肝功能衰竭和死亡,在接受本品治疗期间出现乙型肝炎病毒再活化的患者,应立即停用本品和任何伴随的化疗,并进行适当的治疗,对于乙型肝炎病毒再激活消退的患者,恢复本品治疗应与具有乙型肝炎管理专业知识的医疗保健提供者进行讨论。
接受本品治疗的患者中,考虑进行性多灶性白质脑病的诊断在任何患者出现新的发病或改变原有的神经系统表现,进行性多灶性白质脑病的评估包括但不限于咨询神经科医生,脑MRI和腰椎穿刺,出现进行性多灶性白质脑病,停止本品治疗,并考虑停止或减少任何伴随化疗或免疫抑制治疗的进行性多灶性白质脑病患者。
本品可引起严重和危及生命的输液相关反应,对于先前存在心脏或肺部疾病的患者,在整个输注期间和输注后期间更频繁地监测,因为他们可能有更大的风险经历更严重的反应,低血压可能作为本品输液反应发生因素,考虑在每次输注本品前12小时、输注期间和给药后1小时停止降压治疗,直至血压稳定,对于高血压危象风险增加的患者,考虑停服降压药的益处和风险。
如果在输注过程中或输注后怀疑过敏反应,应停止输注并永久停止治疗。
对于有肿瘤溶解综合征风险的患者,在输注本品之前,应给予适当的抗高尿酸药(如别嘌呤醇或拉布立酶)和水合预防肿瘤溶解,在本品治疗的最初几天,监测被认为有肿瘤溶解综合征风险的患者的实验室参数,对于肿瘤溶解综合征的治疗,纠正电解质异常,监测肾功能和体液平衡,并给予支持性护理,包括必要的透析。
不要给活动性感染的患者使用本品,有复发或慢性感染史的患者感染风险可能增加。
强烈建议中性粒细胞减少严重且持续时间长(>1周)的患者接受抗微生物预防治疗,直至中性粒细胞减少缓解至1级或2级,考虑抗病毒和抗真菌预防。
经常监测所有患者的血小板减少和出血事件,特别是在第一个周期,如果临床指征,评估实验室凝血参数,对于3级或4级血小板减少患者,应更频繁地监测血小板计数,直至解决,并考虑延迟本品和化疗的剂量或减少化疗的剂量,输血血液制品(即血小板输注)可能是必要的,考虑不同时使用可能增加出血风险的药物(血小板抑制剂、抗凝剂),特别是在第一个周期。
对于疑似弥散性血管内凝血的患者,评估潜在原因,监测凝血参数、血小板计数,以及出血或血栓形成的体征和症状,根据弥散性血管内凝血的标准指导方针进行管理,可能需要支持性护理,包括输血和其他医疗管理。
在本品治疗期间或之后接种活疫苗或减毒疫苗的安全性和有效性尚未得到研究,在治疗期间和B细胞恢复之前,不建议接种活病毒疫苗。
基于其作用机制和动物实验结果,本品可导致子宫内暴露于婴儿B细胞耗竭,提醒孕妇注意对胎儿的潜在风险,建议有生殖潜力的女性在接受本品期间和最后一次剂量后6个月内使用有效的避孕措施。
(本内容参考自美国FDA药品说明书2022.07版)
1.如果您发现该药品信息有任何错误,请联系我们修改,我们将热忱感谢您的批评指正!
2.本站所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考!
