



用于多种实体瘤,治疗乳腺癌临床总生存率高
 瑞士罗氏
瑞士罗氏
1.III期结肠癌患者的辅助治疗或联合化疗方案的辅助治疗。
2.局部晚期直肠癌成年患者的围手术期放化疗的组成部分。
3.治疗不可切除或转移性结直肠癌患者的单一用药或联合化疗方案的组成部分。
1.卡培他滨可与多西他赛联合用于治疗含蒽环类药物方案化疗失败的转移性乳腺癌。
2.晚期或转移性乳腺癌患者的单一用药(如果不适合用蒽环类或紫杉类的化疗方案)。
作为联合化疗方案的组成部分用于治疗成人不可切除或转移性胃、食管或胃食管交界癌。
作为联合化疗的一部分用于成人胰腺癌的辅助治疗。
1.应在饭后30分钟内用水整片吞服。
2.药片不需压碎或切割,如果患者无法整片吞服而必须压碎或切割,则应由接受安全操作细胞毒性药物专业培训的人员进行该操作。
1.单一用药时,卡培他滨推荐剂量为1250mg/㎡,每日2次口服(早晚各1次),治疗2周后停药1周,3周为1个疗程。
2.联合多西他赛用药时,卡培他滨推荐剂量为1250mg/㎡,每日2次口服,治疗2周后停药1周,多西他赛推荐剂量为75mg/㎡,每3周1次,1次静脉滴注1小时。
3.联合奥沙利铂用药时,卡培他滨推荐剂量为1000mg/㎡,每日2次口服,治疗2周后停药1周,奥沙利铂推荐剂量为130mg/㎡,静脉输注2小时,奥沙利铂必须在卡培他滨之前完成给药。
4.用于癌灶伴有淋巴结转移患者的辅助治疗时,推荐治疗时间为6个月,即卡培他滨1250mg/㎡,每日2次口服,治疗2周后停药1周,3周为1个疗程,共计8个疗程。
5.联合顺铂用药时,卡培他滨推荐剂量为1000mg/㎡,1天2次,治疗2周后停药1周,顺铂剂80mg/㎡,在每3周疗程的第1天,静脉滴注2小时。
单一用药化疗时剂量调整方案:
不良反应分级1 | 治疗过程中 | 下一疗程剂量调整 (%起始剂量) |
1级 | 维持原剂量 | 维持原剂量 |
2级 | ||
第一次出现 | 暂停用药,直至恢复0-1级 | 100% |
第二次出现 | 暂停用药,直至恢复0-1级 | 75% |
第三次出现 | 暂停用药,直至恢复0-1级 | 50% |
第四次出现 | 永久中止治疗 | |
3级 | ||
第一次出现 | 暂停用药,直至恢复0-1级 | 75% |
第二次出现 | 暂停用药,直至恢复0-1级 | 50% |
第三次出现 | 永久中止治疗 | |
4级 | ||
第一次出现 | 永久中止或遵医嘱 | 50% |
注:1.除手足综合征和高胆红素血症外,使用加拿大临床试验组国家癌症研究所(NCIC)制定的常见毒性反应分级标准(CTC)。
常见不良反应包括腹泻,恶心,呕吐,胃炎,麻木,感觉迟钝,感觉异常,麻刺感,无痛感和疼痛感,皮肤肿胀和红斑,水疱或严重的疼痛等。
1.已知对卡培西滨或其任何辅料过敏者禁用。
2.既往对氟嘧啶有严重、非预期的反应或已知对氟嘧啶过敏患者禁用卡培他滨。
3.卡培他滨禁用于已知二氢嘧啶脱氢酶活性完全缺乏的患者。
4.卡培他滨不应与索立夫定或其类似物(如溴夫定)同时给药。
5.卡培他滨禁用于严重肾功能损伤患者。
6.联合化疗时,如存在任一联合药物相关的禁忌症,则应避免使用该药物。
7.对顺铂的禁忌症同样适用于卡培他滨和顺铂联合治疗。
密封,常温(10~30℃)保存。
成人
1.使用卡培他滨以及同时使用香豆素类衍生物抗凝剂的患者,应常规检测其抗凝参数,并相应调整抗凝剂的剂量。
2.慎与细胞色素P-450 2C9底物共同联用。
3.对使用卡培他滨同时服用苯妥英的患者,应常规检测苯妥英的血浆浓度。
24个月
片剂
瑞士罗氏
本品主要成分为卡培他滨,化学结构式为:
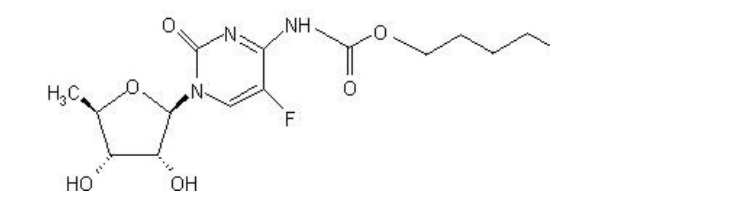
非活性成分为:无水乳糖、交叉碳甲环糖钠、羟丙基甲基纤维素、微晶纤维素、硬脂酸镁和纯化水。桃膜或轻桃膜涂层含有羟丙基甲基纤维素、滑石粉、二氧化钛和合成的黄色和红铁氧化物。
双凸、长方形、桃色或浅桃色包衣片,除去包衣后显白色。
1.卡培他滨可引起腹泻,出现严重腹泻者应给予密切监护。
2.治疗期间可能会造成脱水,此时应及时纠正脱水。
3.使用卡培他滨治疗可能会造成心脏毒性,因此应密切观察患者。
4.已知二氢嘧啶脱氢酶活性完全缺乏的患者不应使用卡培他滨。
5.卡培他滨可能会引起严重皮肤反应,因卡培他滨治疗引起严重皮肤反应的患者应永久停用本品。
6.卡培他滨可能会导致出现手足综合征,出现轻微反应的患者应暂停用药,严重反应患者应减低剂量。
7.卡培他滨可能会引起高胆红素血症,如果药物相关的胆红素升高正常值上限3倍以上或肝转氨酶升高正常值上限2.5倍以上,应暂停使用卡培西滨。
(以上内容参考自中文版说明书2021.05版)
1.如果您发现该药品信息有任何错误,请联系我们修改,我们将热忱感谢您的批评指正!
2.本站所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考!
