

为晚期大肠癌(结直肠癌)的一线用药,也可用于术后的辅助化疗;对肺癌、乳腺癌、胰腺癌等也有一定疗效
推荐预防性给予患者止吐药,当患者出现胆碱能综合症时要考虑预防性或治疗性地给予阿托品治疗
1.盐酸伊立替康与 5-FU(5-氟尿嘧啶)和 LV(亚叶酸钙)联用
两周用药方案 :⑴盐酸伊立替康 180mg/m2 静脉滴注 30~90 分钟,第 1 天
⑵ LV 400mg/m2 应该在盐酸伊立 替康输注后立即给予,滴注时间相同,之后再立即给予 5-FU,第 1 天和第 2 天
⑶ 5-FU 400mg/m2 静脉推注,然后 600mg/m2 持续静脉输注 22 小时,第 1 天和第 2 天,每 2 周重复
⑷盐酸伊立替康 180mg/m2 静脉滴注 30~90 分钟,第 1 天
⑸ LV 400mg/m2 应该在盐酸伊立 替康输注后立即给予,滴注时间相同,第 1 天
⑹ 5-FU 400mg/m2 静脉推注,第 1 天,然后 1,200mg/m2 /d×2 天持续静脉输注(总量 2,400mg/m2 , 输注 46~48 小时),每 2 周重复
表 1 盐酸伊立替康/5-FU/LV 联合治疗周期中和在下一疗程开始时盐酸伊立替康的推荐剂量调整方法
毒性反应 NCI CTC 分级 a | 在治疗周期中 | 下一疗程开始时 b |
没有毒性反应 | 维持剂量水平 | 维持剂量水平 |
中性粒细胞减少 | ||
1
2
3
4 | 维持剂量水平
减少 1 个剂量水平
停药直到恢复至≤2 级,然后减少 1 个剂量水平
停药直到恢复至≤2 级,然后减少 2 个剂量水平 | 维持剂量水平维持剂量水平 减少 1 个剂量水平
减少 2 个剂量水平 |
中性粒细胞减少性发热 | 停药直到恢复, ,然后减少 2 个剂量水平 | |
其它血液系统毒性 | 在某一治疗周期中和下一疗程开始时,根据白细胞减少和血小板减少进行的剂 量调整也要基于 NCI 毒性评估标准,并且与上述中性粒细胞减少推荐的剂量调 整方案一致 | |
腹泻 | ||
1
2
3
4 | 延迟用药直至恢复至基线水平,然后给予相同 的剂量,
停止用药直至恢复至基线水平,然后减少 1 个剂量水平
停止用药直至恢复至基线水平,然后减少 1 个剂量水平
停止用药直至恢复至基线水平,然后减少 2 个剂量水平 | 维持剂量水平
维持剂量水平
减少 1 个剂量水平
减少 2 个剂量水平 |
其它非血液系统毒性 c | ||
1
2
3
4 | 维持剂量水平
停药直到恢复至≤1 级,然后减少 1 个剂量水平
停药直到恢复至≤2 级,然后减少 1 个剂量水平
停药直到恢复至≤2 级,然后减少 2 个剂量水平 | 维持剂量水平维持剂量水平
减少 1 个剂量水平
减少 2 个剂量水平 |
a 基于 NCI CTC (version 2.0)标准评估不良事件的严重性
b 相对于先前化疗周期中使用的起始剂量
c 对于粘膜炎/口腔炎只要减少 5-FU 剂量,不需减少盐酸伊立替康剂量
肝功能异常的患者,推荐以下起始剂量:
表 2:有肝功能异常患者的起始剂量-单药方案
方案 | 血清总胆红素浓度 | 血清 ALT/AST 浓度 | 起始剂量, mg/m2 |
单药每周方案 | 1.5 – 3.0 x IULN | ≤5.0 x IULN | 60 |
3.1 – 5.0 x IULN | ≤5.0 x IULN | 50 | |
<1.5 x IULN | 5.1 – 20.0 x IULN | 60 | |
1.5 – 5.0 x IULN | 5.1 – 20.0 x IULN | 40 | |
单药每 3 周一次方案 | 1.5 – 3.0 x IULN | - | 200 |
> 3.0 x IULN | - | 不推荐 a |
a 在胆红素>3.0 x IULN 的患者中,盐酸伊立替康每 3 周一次给药方案的安全性和药代动力学尚不明确,而且该方案不推荐在这类患者中使用
1.与其他注射用药一样,本品溶液的配制必须严格遵循无菌原则
2.盐酸伊立替康注射液只能一次性使用,任何未使用的部分必须丢弃
3.盐酸伊立替康注射液在输注之前必须用 5%葡萄糖注射液或 0.9%氯化钠注射液稀释至终浓度为 0.12 至 2.8mg/ml 的输注液。其它药物不能加入输注液中,只要溶液和容器允许, 应在输注之前检查输注液中是否有可见的颗粒物质和变色,检查药瓶中是否有颗粒物质,当药物从药瓶中抽入注射器时再检查一遍
4.在 5°C 或 30°C/相对湿度和避光条件下,盐酸伊立替康注射液稀释于输注液(0.9%氯化钠溶液和 5%葡萄糖溶液)并贮藏在低密度聚乙烯或聚氯乙烯容器中,其化学和物理稳定性可保持 28 天,如在光照条件下其化学和物理稳定性可保持 3 天
5.然而为了减少微生物感染的风险,推荐在使用之前才准备输注液,而且输注液准备好后应尽快使用,如果未立即使用,输注液在 2-8°C 条件下贮藏时间不应超过 24 小时,或在室温条件下(25°C)贮藏时间不超过 6 小时
6.不要冰冻盐酸伊立替康或其溶液混合物,因为这可能导致药物沉淀形成
常见的不良反应有恶心、食欲下降、反胃、消化不良、延迟性腹泻、中性粒细胞减少、免疫力下降、对肝脏造成较大的负担
1.慢性肠炎和(或)肠梗阻的患者禁用
2.对盐酸伊立替康三水合物或其辅料有严重过敏反应史的患者禁用
3.孕妇和哺乳期妇女禁用。胆红素超过正常值上限1.5倍的患者禁用
4.严重骨髓功能衰竭的患者禁用
5.WHO行为状态评分﹥2的患者禁用
遮光、密封、干燥处保存
成人(孕妇和哺乳期妇女禁用)
同时接受酮康唑治疗会引起盐酸伊立替康的清除率显著下降,导致其活性代谢产物 SN-38 暴露增加,可能导致不良反应概率及严重程度增加,在开始盐酸伊立替康治疗前至少一周应停止使用酮康唑,也不能与盐酸伊立替康一同给药
同时使用阿扎那韦,一种 CYP3A4 和 UGT1A1 的抑制剂,可能使伊立替康的活性代谢产物 SN-38 暴露增加,可能导致不良反应概率及严重程度增加,医师在同时使用这些药物的时候要考虑到这一点
⑴抗惊厥剂:合并使用 CYP3A 诱导的抗惊厥剂(如卡马西平、苯巴比妥或苯妥英)会引起 SN-38 暴露减少,疗效降低,对于需要抗惊厥剂治疗的患者,应该考虑在初次使用盐酸伊立替康治疗之前至少一周开始或换用非酶诱导的抗惊厥剂
⑵St. John’s Wort(贯叶连翘):在同时接受贯叶连翘治疗的患者,活性代谢产物 SN-38 的暴露减少,疗效降低,在初次使用盐酸伊立替康前至少一周停用贯叶连翘,该药也不能与盐酸伊立替康同时使用
36个月
注射剂
美国辉瑞
本品主要有效成分为:盐酸伊立替康
其化学结构如下:
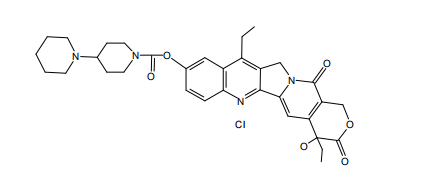
淡黄色至黄色的疏松块状物或粉末
本品须在有使用细胞毒化疗药物经验的肿瘤专科医师的监督指导下使用,只有在能方便地获得充足的诊断和治疗设备的情况下,才可能给予并发症恰当的处理
本品是通过静脉滴注给药的,需要注意防止外渗,静滴部位要注意观察是否有炎症发生,一旦发生外渗,用无菌水冲洗并推荐给予冰敷
由于使用化疗药物包括盐酸伊立替康而导致免疫功 能低下的患者接种活疫苗或减毒活疫苗,可能导致严重或致命的感染,使用盐酸伊立替康的患者应当避免接种活疫苗,可以接种死疫苗或灭活疫苗,但是可能会减弱疫苗的疗效
使用本品的患者血栓事件罕有发生,具体发生的原因仍然不明
1.如果您发现该药品信息有任何错误,请联系我们修改,我们将热忱感谢您的批评指正!
2.本站所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考!
